<ミクロな粒子>
Update 2024.11.14
|
9.ミクロな粒子 超々微小の物質を構成する素粒子 → まとめ 10.放射線 放射線と原子力、放射性物質、宇宙線 11.元素と周期表 元素記号一覧、周期表、周期表の仕組み、電子配置 12.量子論 ミクロの世界の不思議なルール |
| 素粒子 | フェルミ粒子 (基本粒子) | 物質粒子 | 第1世代 | 第2世代 | 第3世代 | 電荷 | スピン |
|---|---|---|---|---|---|---|---|
| クォーク (ハドロン構成粒子) | u(アップ) | c(チャーム) | t(トップ) | 2/3 | 1/2 | ||
| d(ダウン) | s(ストレンジ) | b(ボトム) | -1/3 | ||||
| レプトン (軽粒子) | 電子e-,陽電子e+ | ミュー粒子μ± | タウ粒子τ± | ±1 | |||
| 電子ニュートリノνe | ミューニュートリノνμ | タウニュートリノντ | 0 | ||||
| ボース粒子 | 力の伝達粒子 | 電磁相互作用 | 弱い相互作用 | 強い相互作用 | 電荷 | スピン | |
| ゲージ粒子 (力の粒子) | フォトン (γ:光子) | 弱ボソン (W±,Z) | グルーオン (g:膠着子) | (注1) | 1 | ||
| 粒子に質量を与える粒子 | 電荷 | スピン | |||||
| スカラー粒子 | ヒッグス粒子(H) | 0 | 0 | ||||
| 複合粒子 | ハドロン (強粒子) | バリオン (重粒子) | 核子(陽子p,中性子n),デルタ粒子⊿ | (計算) | (注2) | ||
| ハイペロン(ラムダ粒子Λ,シグマ粒子Σ,グザイ粒子Ξ,オメガ粒子Ω) | (計算) | (注3) | |||||
| メソン(中間子) | π,η,ρ,ω,φ,J/ψ,Y,K,B,D | (計算) | (注4) | ||||
| その他 | 原子核,ハイパー核,原子,分子,イオンなど | ||||||
注1:Wボソンは電荷±1、それ以外のゲージ粒子は電荷0
注2:核子はスピン1/2、デルタ粒子はスピン3/2
スピンが3/2ということは、デルタ粒子を構成する3つのクォークは、3つのうち1つが反対の
方向を向いている核子とは異なり、全て同じ方向を向いていることを示している
デルタ粒子は強い力の作用で瞬時に核子に変わる
注3:ハイペロンはストレンジ粒子とも言われ、奇妙さに応じsクォークを1~3個もつ
オメガ粒子はスピン3/2、それ以外のハイペロンはスピン1/2
ハイペロンは弱い力の作用で中間子を放出して、ゆっくりと核子に変わる
注4:擬スカラー中間子はスピン0:π中間子,η中間子など
ベクター中間子はスピン1:ρ中間子,ω中間子,φ中間子,J/ψ中間子,Υ中間子など
K,D,B中間子は荷電の有無や構成クォ―クで擬スカラー中間子またはベクター中間子に属す
上記以外:仮説上の素粒子(重力子など),仮説上の複合粒子,準粒子他多数のハドロンが発見されている
核子や中間子のように核力を感じる物質粒子を「強粒子(ハドロン、hadron)」と総称
核力は感じないものの、電磁気力と弱い力を感じる物質粒子を「軽粒子(レプトン、lepton)」と総称
上記の表のうち素粒子の部分を標準理論(標準模型)といいます
しかし、自然を完璧に記述していると言う訳ではありません
重力を説明できていませんし、
天体観測でその存在が確認されているダークマターも説明できません
物質の他に反物質(反対の電荷をもつ物質)を説明することはできますが、
星や銀河が物質でできていて、なぜ反物質ではないのか、その理由は説明できていません
注2:核子はスピン1/2、デルタ粒子はスピン3/2
スピンが3/2ということは、デルタ粒子を構成する3つのクォークは、3つのうち1つが反対の
方向を向いている核子とは異なり、全て同じ方向を向いていることを示している
デルタ粒子は強い力の作用で瞬時に核子に変わる
注3:ハイペロンはストレンジ粒子とも言われ、奇妙さに応じsクォークを1~3個もつ
オメガ粒子はスピン3/2、それ以外のハイペロンはスピン1/2
ハイペロンは弱い力の作用で中間子を放出して、ゆっくりと核子に変わる
注4:擬スカラー中間子はスピン0:π中間子,η中間子など
ベクター中間子はスピン1:ρ中間子,ω中間子,φ中間子,J/ψ中間子,Υ中間子など
K,D,B中間子は荷電の有無や構成クォ―クで擬スカラー中間子またはベクター中間子に属す
上記以外:仮説上の素粒子(重力子など),仮説上の複合粒子,準粒子他多数のハドロンが発見されている
核子や中間子のように核力を感じる物質粒子を「強粒子(ハドロン、hadron)」と総称
核力は感じないものの、電磁気力と弱い力を感じる物質粒子を「軽粒子(レプトン、lepton)」と総称
上記の表のうち素粒子の部分を標準理論(標準模型)といいます
しかし、自然を完璧に記述していると言う訳ではありません
重力を説明できていませんし、
天体観測でその存在が確認されているダークマターも説明できません
物質の他に反物質(反対の電荷をもつ物質)を説明することはできますが、
星や銀河が物質でできていて、なぜ反物質ではないのか、その理由は説明できていません
○生体の構成:生き物─→器官─→組織─→細胞小器官─→組織化された高分子─→分子や原子
オルガネラ 高分子:タンパク質,核酸,多糖類
オルガネラ 高分子:タンパク質,核酸,多糖類
| / → \ |
| / → \ |
| / → \ |
| / → \ |
| ||||||||||
|
10倍に拡大 | ↑| 10倍に拡大 | ↑↑
【ピンポン玉:水素原子】 ≒ 【地球:ピンポン玉】| || └→1千倍に拡大→┘| | || | └→1万倍に拡大→┘└─────→1万倍に拡大─────→┘ 【原子:原子核】 ≒ 【甲子園球場:1円玉】 | ||||||||||||||||||
原子・分子の世界:電子を動かす電気の力を伝える光子、電子と光子が主役
原子核・素粒子の世界:太陽や宇宙や超高温・高エネルギー現象、究極の粒子
原子核の大きさは原子の1万分の1、原子核の比重は原子の比重の数兆倍程度
原子核・素粒子の世界:太陽や宇宙や超高温・高エネルギー現象、究極の粒子
原子核の大きさは原子の1万分の1、原子核の比重は原子の比重の数兆倍程度
陰極線の発見─┬→電磁波の発見→X線の発見→放射線の発見→原子核の発見
│ (原子にα線照射)
└→電子の発見(陰極線は電子)
陽子の発見→中性子の発見→中間子の発見→ニュートリノの発見│ (原子にα線照射)
└→電子の発見(陰極線は電子)
反陽子の発見→クォークの存在予言と発見→ヒッグス粒子の発見
電子以外の素粒子は20世紀に発見、ヒッグス粒子は2012年に発見
核子は3つのクォークからなる複合粒子、中間子はクォークと反クォークからなる複合粒子
クォーク:((u,d),(c,s),(t,b))、反クォーク:((反u,反d),(反c,反s),(反t,反b))
クォーク:((u,d),(c,s),(t,b))、反クォーク:((反u,反d),(反c,反s),(反t,反b))
素粒子の電荷:(u,c,t)クォーク=2/3、(d,s,b)クォーク=-1/3、(e,μ,τ)=±1、ν=0
ハドロンの電荷:陽子(uud)=1、中性子(udd)=0、デルタ粒子(uuu,uud,udd,ddd)=(2,1,0,-1)、
π+中間子(u反d)=1、π-中間子(d反u)=-1、π0中間子=(u反u)or(d反d)=0
ラムダ粒子(uds)、シグマ粒子(uus,uds,dds)、グザイ粒子(uss,dss)、オメガ粒子(sss)
Λ( 0)、 Σ( 1, 0, -1)、 Ξ( 0, -1)、 Ω( -1)
ハドロンの電荷:陽子(uud)=1、中性子(udd)=0、デルタ粒子(uuu,uud,udd,ddd)=(2,1,0,-1)、
π+中間子(u反d)=1、π-中間子(d反u)=-1、π0中間子=(u反u)or(d反d)=0
ラムダ粒子(uds)、シグマ粒子(uus,uds,dds)、グザイ粒子(uss,dss)、オメガ粒子(sss)
Λ( 0)、 Σ( 1, 0, -1)、 Ξ( 0, -1)、 Ω( -1)
粒子と電荷が反対の反粒子が出会うと中間子や光子を放出して消滅する(クォークと反クォークが消滅する)
中間子はクォークと反クォークからなり、中間子と核子、+中間子と-中間子が別の核子や別の中間子になる
陽子(uud)+π-中間子(d,反u)=中性子(udd)、中性子(udd)+π+中間子(u,反d)=陽子(uud)
陽子(uud)=中性子(udd)+π+中間子(u,反d)、中性子(udd)=陽子(uud)+π-中間子(d,反u)
K+中間子(u,反s)+K-中間子(反u,s)=Φ中間子(s,反s)
バリオン:クォーク3つでできた白色状態、バリオンの反粒子反バリオン:反クォーク3つでできた白色状態
中間子はクォークと反クォークからなり、中間子と核子、+中間子と-中間子が別の核子や別の中間子になる
陽子(uud)+π-中間子(d,反u)=中性子(udd)、中性子(udd)+π+中間子(u,反d)=陽子(uud)
陽子(uud)=中性子(udd)+π+中間子(u,反d)、中性子(udd)=陽子(uud)+π-中間子(d,反u)
K+中間子(u,反s)+K-中間子(反u,s)=Φ中間子(s,反s)
バリオン:クォーク3つでできた白色状態、バリオンの反粒子反バリオン:反クォーク3つでできた白色状態
原子や分子、素粒子などの量子状態を表わす数値として、量子力学で使われる各種の「量子数」がある
量子状態とは電子のような粒子を見分けるための量子数の組み合わせ(=個体識別データ)
電子の量子状態を決める量子数は次の4種類:電子が原子核のまわりを公転する電子軌道を決定する①②③
①主量子数n :軌道の大きさ(原子核・電子間の距離、電子殻:K,L,M,N,…殻)n=1,2,…,7
②方位量子数l:軌道の形 (円・楕円、電子軌道の種類:spdf軌道)l=0,1,2,…,n-1
③磁気量子数m:軌道の向き (軌道の立体的な角度:電子軌道は磁場の中にある)-l≦m≦l
④スピンs :磁気的な性質(電子の自転?回転角運動量?電子の磁気?)+1/2,-1/2
粒子には電荷や性質(内部量子数)の符号が反対の粒子(=反粒子)があるが、区別のない光子などもある
内部量子数(運動量や座標によらない量子数):フレーバー(6種のクォーク),電荷,バリオン数,レプトン数等
2種のクォークは3世代で6種のフレーバー、3種の色の状態、スピンが2種の回り方で計36種類の状態です
量子状態とは電子のような粒子を見分けるための量子数の組み合わせ(=個体識別データ)
電子の量子状態を決める量子数は次の4種類:電子が原子核のまわりを公転する電子軌道を決定する①②③
①主量子数n :軌道の大きさ(原子核・電子間の距離、電子殻:K,L,M,N,…殻)n=1,2,…,7
②方位量子数l:軌道の形 (円・楕円、電子軌道の種類:spdf軌道)l=0,1,2,…,n-1
③磁気量子数m:軌道の向き (軌道の立体的な角度:電子軌道は磁場の中にある)-l≦m≦l
④スピンs :磁気的な性質(電子の自転?回転角運動量?電子の磁気?)+1/2,-1/2
粒子には電荷や性質(内部量子数)の符号が反対の粒子(=反粒子)があるが、区別のない光子などもある
内部量子数(運動量や座標によらない量子数):フレーバー(6種のクォーク),電荷,バリオン数,レプトン数等
2種のクォークは3世代で6種のフレーバー、3種の色の状態、スピンが2種の回り方で計36種類の状態です
フェルミ粒子:クォーク,レプトン,核子(陽子,中性子) … スピンが半整数になるのがフェルミオン
ボース粒子 :ゲージ粒子,重力子,ヒッグス粒子,中間子 … スピンが整数になるのがボソン
パウリの排他律:ボース粒子は重ねられるけれどフェルミ粒子は重ねられない(スピンが性格を決める)
・ボース粒子 :2個以上の粒子が同じ状態をとれる (同じ位置に重ねられる、 空間的大きさがない)
・フェルミ粒子:一つの状態を1個の粒子しかとれない(同じ位置に重ねられない、空間的大きさがある)
ボース粒子 :ゲージ粒子,重力子,ヒッグス粒子,中間子 … スピンが整数になるのがボソン
パウリの排他律:ボース粒子は重ねられるけれどフェルミ粒子は重ねられない(スピンが性格を決める)
・ボース粒子 :2個以上の粒子が同じ状態をとれる (同じ位置に重ねられる、 空間的大きさがない)
・フェルミ粒子:一つの状態を1個の粒子しかとれない(同じ位置に重ねられない、空間的大きさがある)
ボース粒子は極低温でボース・アインシュタイン凝縮(BEC理論)を起こす
ある転移温度以下で巨視的な数のボース粒子がある1つの1粒子状態に落ち込む相転移現象
ボース粒子であるヘリウム4はその凝縮を起源とする超流動状態(粘性ゼロ)を示す
フェルミ粒子2個は疑似ボース粒子としてボース・アインシュタイン凝縮を起こす
電子の対はその凝縮を起源とする超伝導状態(電気抵抗ゼロ)を示す … 電荷を持った粒子の超流動
ヘリウム3の対はその凝縮を起源とする超流動状態を示す
ある転移温度以下で巨視的な数のボース粒子がある1つの1粒子状態に落ち込む相転移現象
ボース粒子であるヘリウム4はその凝縮を起源とする超流動状態(粘性ゼロ)を示す
フェルミ粒子2個は疑似ボース粒子としてボース・アインシュタイン凝縮を起こす
電子の対はその凝縮を起源とする超伝導状態(電気抵抗ゼロ)を示す … 電荷を持った粒子の超流動
ヘリウム3の対はその凝縮を起源とする超流動状態を示す
素粒子のスピンは大きさと向きをもち、クォークのスピンの大きさは1/2,向きは右回りが(+),左回りが(-)
核子のスピン:核子内の3つのクォークのうち2つは右回り(+)、1つは左回り(-)で、全体で右回り(+)の
スピン1/2です:+1/2+1/2-1/2=+1/2 … uクォークが+、dクォークが-ではなく、各々+か-がある
ラムダ粒子はuクォークとdクォークのスピンが逆で打ち消しあいラムダ粒子のスピンはsクォークのスピンです
デルタ粒子は3つのクォークのスピンの向きが同じ(左/右)3/2
核子は特定のエネルギーの光子を吸収して左回りの1つが右回りになりスピンの向きが同じデルタ粒子になる
電荷がありスピンしているクォークはミニ磁石で、クォーク磁石が3つ合わさって核子の磁石になる
核子のスピン:核子内の3つのクォークのうち2つは右回り(+)、1つは左回り(-)で、全体で右回り(+)の
スピン1/2です:+1/2+1/2-1/2=+1/2 … uクォークが+、dクォークが-ではなく、各々+か-がある
ラムダ粒子はuクォークとdクォークのスピンが逆で打ち消しあいラムダ粒子のスピンはsクォークのスピンです
デルタ粒子は3つのクォークのスピンの向きが同じ(左/右)3/2
核子は特定のエネルギーの光子を吸収して左回りの1つが右回りになりスピンの向きが同じデルタ粒子になる
電荷がありスピンしているクォークはミニ磁石で、クォーク磁石が3つ合わさって核子の磁石になる
電子のスピンは上向きスピンと下向きスピンの2種類
パウリの排他原理:ひとつの電子軌道に入れる電子は2個までで、そのスピンは逆でなければならない
同じ量子状態の共有を禁ずるのがパウリの排他原理
最低ひとつの量子数は違っていなければならない、軌道が同じならスピンは異なってなくてはならない
ひとつの電子軌道に複数の電子が入るにはスピンが違っていなければならないしスピンは2通りしかない
ひとつの電子軌道に入れる電子は互いにスピンが逆のふたつだけ
電荷がありスピンしている電子はミニ磁石です(電流と磁界の向きはアンペールの右ねじの法則に従う)
上向きスピンは下から見て右回り(+)でN極が上、下向きスピンは下から見て左回り(-)でN極が下
アンペール、ビオ・サバール ファラデー、フレミング
パウリの排他原理:ひとつの電子軌道に入れる電子は2個までで、そのスピンは逆でなければならない
同じ量子状態の共有を禁ずるのがパウリの排他原理
最低ひとつの量子数は違っていなければならない、軌道が同じならスピンは異なってなくてはならない
ひとつの電子軌道に複数の電子が入るにはスピンが違っていなければならないしスピンは2通りしかない
ひとつの電子軌道に入れる電子は互いにスピンが逆のふたつだけ
電荷がありスピンしている電子はミニ磁石です(電流と磁界の向きはアンペールの右ねじの法則に従う)
上向きスピンは下から見て右回り(+)でN極が上、下向きスピンは下から見て左回り(-)でN極が下
N S
→ ▲ ← △
+1/2 ↑○↓ ◎ -1/2 ↓○↑ ◎
← ▽ → ▼
S N
「電流と磁界に関する法則」と「電磁誘導に関する法則」は別ものなので混同しないようにしましょう→ ▲ ← △
+1/2 ↑○↓ ◎ -1/2 ↓○↑ ◎
← ▽ → ▼
S N
アンペール、ビオ・サバール ファラデー、フレミング
デルタ++粒子は3つのクォークが、同じ電荷+2/3の状態、同じuのフレーバーの状態、同じスピンの向きで、
同じ場所にあり、パウリの排他原理に違反しないためには3つの異なる色の状態が必要になる
クォークの新しい3種の状態として、赤・青・緑の3原色が考えられた
オメガ-粒子内の3つのクォークも同じsフレーバー、同じ-1/3電荷ですが、3つの異なる色の状態をもつ
核子・デルタ粒子・ハイペロンなどの重粒子は3つのクォークが3つの色の衣を持ち、中間子はクォーク
・反クォークが2つの補色関係の色の衣をもつ(クォークや中間子の色の衣は時々衣を交換する)
クォークの閉じ込め:クォークが単独では存在しないのは、色は単色では存在できず、無色の粒子だけが
単独で存在できる事や、単独の分数電荷では存在できず、整数電荷だけが単独で存在できる事を意味する
同じ場所にあり、パウリの排他原理に違反しないためには3つの異なる色の状態が必要になる
クォークの新しい3種の状態として、赤・青・緑の3原色が考えられた
オメガ-粒子内の3つのクォークも同じsフレーバー、同じ-1/3電荷ですが、3つの異なる色の状態をもつ
核子・デルタ粒子・ハイペロンなどの重粒子は3つのクォークが3つの色の衣を持ち、中間子はクォーク
・反クォークが2つの補色関係の色の衣をもつ(クォークや中間子の色の衣は時々衣を交換する)
クォークの閉じ込め:クォークが単独では存在しないのは、色は単色では存在できず、無色の粒子だけが
単独で存在できる事や、単独の分数電荷では存在できず、整数電荷だけが単独で存在できる事を意味する
フェルミ粒子:軽い順に第1世代,第2世代,第3世代と呼ぶが、現在の原子の構成要素は第1世代のみ
他の世代は、宇宙創成時に存在したが現在の地球にはなく、加速粒子を衝突させて、人工的に作られる
ミュー粒子は、宇宙線が大気中の原子と衝突して生成され地表に到達する2次宇宙線として観測される
世代が高い粒子は、それより前の世代の対応する粒子よりも大きな質量を持つ … 質量階層
各世代間は、粒子の質量のみ異なり、全ての基本相互作用および量子数は同一
他の世代は、宇宙創成時に存在したが現在の地球にはなく、加速粒子を衝突させて、人工的に作られる
ミュー粒子は、宇宙線が大気中の原子と衝突して生成され地表に到達する2次宇宙線として観測される
世代が高い粒子は、それより前の世代の対応する粒子よりも大きな質量を持つ … 質量階層
各世代間は、粒子の質量のみ異なり、全ての基本相互作用および量子数は同一
核子と高エネルギーの中間子や光子の衝突でハイペロン(ストレンジ粒子)が作られる
ラムダ粒子(uds),シグマ粒子(uus,uds,dds),グザイ粒子(uss,dss),オメガ粒子(sss)
核子内の3つのクォークのうち1個~3個がsクォークであるのがハイペロンです
ハイペロンを含む原子核をハイパー核と言い、ハイパー核内のハイペロンは弱い力
の作用で陽子や中性子に変わり、ハイパー核は通常の原子核に戻る
ラムダ粒子(uds),シグマ粒子(uus,uds,dds),グザイ粒子(uss,dss),オメガ粒子(sss)
核子内の3つのクォークのうち1個~3個がsクォークであるのがハイペロンです
ハイペロンを含む原子核をハイパー核と言い、ハイパー核内のハイペロンは弱い力
の作用で陽子や中性子に変わり、ハイパー核は通常の原子核に戻る
レプトンの各世代は弱い力の作用で±W弱ボソンを交換して変換する(ただし同世代の中に限る)
電荷を持つ粒子と電荷を持たない粒子間で双方向に変換する(e⇔νe、μ⇔νμ、τ⇔ντ)
μ粒子は百万分の22秒の寿命でμニュートリノに変わり、電子と反電子ニュートリノを放出する
τ粒子は10兆分の3秒の寿命でτニュートリノに変わり、電子と反電子ニュートリノを放出する
か、μ粒子と反μニュートリノを放出する
電荷を持つ粒子と電荷を持たない粒子間で双方向に変換する(e⇔νe、μ⇔νμ、τ⇔ντ)
μ粒子は百万分の22秒の寿命でμニュートリノに変わり、電子と反電子ニュートリノを放出する
τ粒子は10兆分の3秒の寿命でτニュートリノに変わり、電子と反電子ニュートリノを放出する
か、μ粒子と反μニュートリノを放出する
ニュートリノには電子ニュートリノ、μニュートリノ、τニュートリノの3種類があります
これは「フレーバー」による分類です … 電子型νe、ミュー型νμ、タウ型ντ
ニュートリノは物質に当たって弱い相互作用を受けると、荷電レプトンに変わります
・電子に変わるニュートリノを電子ニュートリノ
・μ粒子に変わるニュートリノをμニュートリノ
・τ粒子に変わるニュートリノをτニュートリノ
3種類の荷電レプトン(e,μ,τ) : 質量でのみ識別可能
3種類のニュートリノ : 物質と相互作用することによって識別可能=フレーバー
一方、ニュートリノは「質量」という分類で分けることもできます
m1,m2,m3という3つの異なる質量を持つ、
ニュートリノ1、ニュートリノ2、ニュートリノ3の3種類です … ν1、ν2、ν3
ニュートリノ混合:ニュートリノν1、ν2、ν3の混合
νe=[ν1>ν2>ν3]、νμ=[ν1<ν2≒ν3]、ντ=[ν1<ν2<ν3]
ニュートリノは、異なる質量を持つ複数の可能性が重ね合わさった状態
これは「フレーバー」による分類です … 電子型νe、ミュー型νμ、タウ型ντ
ニュートリノは物質に当たって弱い相互作用を受けると、荷電レプトンに変わります
・電子に変わるニュートリノを電子ニュートリノ
・μ粒子に変わるニュートリノをμニュートリノ
・τ粒子に変わるニュートリノをτニュートリノ
3種類の荷電レプトン(e,μ,τ) : 質量でのみ識別可能
3種類のニュートリノ : 物質と相互作用することによって識別可能=フレーバー
一方、ニュートリノは「質量」という分類で分けることもできます
m1,m2,m3という3つの異なる質量を持つ、
ニュートリノ1、ニュートリノ2、ニュートリノ3の3種類です … ν1、ν2、ν3
ニュートリノ混合:ニュートリノν1、ν2、ν3の混合
νe=[ν1>ν2>ν3]、νμ=[ν1<ν2≒ν3]、ντ=[ν1<ν2<ν3]
ニュートリノは、異なる質量を持つ複数の可能性が重ね合わさった状態
①原子炉内の核分裂の際の放射性核のベータ変換、②高エネルギー陽子加速器で生成(下図)
③宇宙、超新星、太陽、大気、地球の裏側、人体からやってくる
電気を帯びずよく透過する、弱い力だけが作用する、電子の100万分の1以下の質量
現時点では、左巻きらせん運動のニュートリノと、右巻きらせん運動の反ニュートリノ
しか見つかっていない(他の素粒子は、粒子は左右あり、反粒子も左右ある)
↑ ↑
π+中間子→μ+粒子→e+
↑ ↓
500MeV │ νe
②高エネルギー陽子→Be原子核
│ νe
↓ ↑
π-中間子→μ-粒子→e-
↓ ↓
νμ νμ
③太陽風陽子の場合→大気中の窒素や酸素→…ミュー粒子、電子、ニュートリノ
③宇宙、超新星、太陽、大気、地球の裏側、人体からやってくる
電気を帯びずよく透過する、弱い力だけが作用する、電子の100万分の1以下の質量
現時点では、左巻きらせん運動のニュートリノと、右巻きらせん運動の反ニュートリノ
しか見つかっていない(他の素粒子は、粒子は左右あり、反粒子も左右ある)
①核反応パイ中間子の変換によるニュートリノ生成
νμ νμ↑ ↑
π+中間子→μ+粒子→e+
↑ ↓
500MeV │ νe
②高エネルギー陽子→Be原子核
│ νe
↓ ↑
π-中間子→μ-粒子→e-
↓ ↓
νμ νμ
③太陽風陽子の場合→大気中の窒素や酸素→…ミュー粒子、電子、ニュートリノ
ニュートリノは、「粒子」であると同時に「波」としての性質を持ちます
それぞれ異なる質量を持つニュートリノν1、ν2、ν3は、
それぞれ異なる振動数を持つ「波」として空間を伝播します
ニュートリノのフレーバーは、3種類の質量の決まった「波」の「重ね合わせ」(合成波)となり、
ニュートリノが空間を飛ぶ間に合成波の位相が変化し、フレーバーの種類(型)が移り変わります
νe⇔νμ、νμ⇔ντ、ντ⇔νe この現象をニュートリノ振動と呼びます
ニュートリノが質量を持ち、ゼロではないニュートリノ混合があるときに起こる現象です
質量がわずかに異なる3種類のニュートリノν1、ν2、ν3は、それぞれ異なる速度で飛行する
これを飛行経路のある場所で観測すると、元々作られた型とは異なるタイプのニュートリノに、
ある確率で変わってしまう … ニュートリノの世代交代(移動)が起こる
ニュートリノ振動が起きる割合はν1、ν2、ν3の質量の二乗の差と飛行距離に比例し、
ニュートリノが持つエネルギーに反比例する
ニュートリノが反応した時に対になっている、電子やμ粒子、τ粒子を観測し、
ニュートリノの型を判別することで型の変化がわかります(型:フレーバーによる分類)
それぞれ異なる質量を持つニュートリノν1、ν2、ν3は、
それぞれ異なる振動数を持つ「波」として空間を伝播します
ニュートリノのフレーバーは、3種類の質量の決まった「波」の「重ね合わせ」(合成波)となり、
ニュートリノが空間を飛ぶ間に合成波の位相が変化し、フレーバーの種類(型)が移り変わります
νe⇔νμ、νμ⇔ντ、ντ⇔νe この現象をニュートリノ振動と呼びます
ニュートリノが質量を持ち、ゼロではないニュートリノ混合があるときに起こる現象です
質量がわずかに異なる3種類のニュートリノν1、ν2、ν3は、それぞれ異なる速度で飛行する
これを飛行経路のある場所で観測すると、元々作られた型とは異なるタイプのニュートリノに、
ある確率で変わってしまう … ニュートリノの世代交代(移動)が起こる
ニュートリノ振動が起きる割合はν1、ν2、ν3の質量の二乗の差と飛行距離に比例し、
ニュートリノが持つエネルギーに反比例する
ニュートリノが反応した時に対になっている、電子やμ粒子、τ粒子を観測し、
ニュートリノの型を判別することで型の変化がわかります(型:フレーバーによる分類)
| 素粒子・複合粒子 | 第1世代 | ||
|---|---|---|---|
| 素粒子 | フェルミ粒子 (基本粒子) | クォーク (ハドロン構成粒子) | u(アップ) |
| d(ダウン) | |||
| レプトン (軽粒子) | 電子e-,陽電子e+ | ||
| 電子ニュートリノνe | |||
| ボース粒子 | ゲージ粒子 (力の粒子) | 光子,弱ボソン(W±,Z) グルーオン(g:膠着子) | |
| スカラー粒子 | ヒッグス粒子(H) | ||
| 複合粒子 | ハドロン (強粒子) | バリオン (重粒子) | 核子(陽子uud,中性子udd) デルタ粒子(uuu,uud,udd,ddd) |
| メソン (中間子) | π+ ,π- ,π0 u反d,d反u,(u反u)or(d反d) | ||
| その他 | 原子核 | ||
フェルミ粒子:クォーク,レプトン,核子(陽子,中性子)
ボース粒子 :ゲージ粒子,重力子,ヒッグス粒子,中間子
量子数 :粒子の量子状態を表わす数値(電荷やスピン)
ボース粒子 :ゲージ粒子,重力子,ヒッグス粒子,中間子
量子数 :粒子の量子状態を表わす数値(電荷やスピン)
二次宇宙線 :ミュー粒子は50万分の1秒の寿命ですが特殊相対性理論で10倍延びて地表に到達する
現存する核子を構成するクォークは第1世代のみで、現存する原子を構成する電子も第1世代である
他の世代のクォークやレプトンは宇宙創成時には存在したが現在の地球にはなく、人工的に作られる
物質の占める割合は多くなく宇宙の全質量の大部分は未知の物質で見えないので暗黒物質と呼ばれる
ニュートリノはいまだに謎の多い粒子でニュートリノの正体と暗黒物質の探索が活発に行われている
現存する核子を構成するクォークは第1世代のみで、現存する原子を構成する電子も第1世代である
他の世代のクォークやレプトンは宇宙創成時には存在したが現在の地球にはなく、人工的に作られる
物質の占める割合は多くなく宇宙の全質量の大部分は未知の物質で見えないので暗黒物質と呼ばれる
ニュートリノはいまだに謎の多い粒子でニュートリノの正体と暗黒物質の探索が活発に行われている
| 種類 | 放射線 | |
|---|---|---|
| 粒子線 | アルファ線 | ヘリウム原子核、電荷:+2 |
| 放射性原子核はアルファ変換で陽子2個中性子2個減り質量数4少ない原子核になる | ||
| ベータ線 | 電子・陽電子、電荷:±1 | |
| 電子が出るベータ変換では、放射性原子核の中性子が陽子になる | ||
| 陽電子が出るベータ変換では、放射性原子核の陽子が中性子になる | ||
| 電子や陽電子が出るベータ変換では、もう一つの粒子ニュートリノが放出される | ||
| 陽子線 | 陽子線:水素の原子核、重陽子線:重水素の原子核、電荷:+1 | |
| 人工的に原子核反応を起こす加速器等から作られる | ||
| 中性子線 | 核分裂などの際に核外に飛び出す中性子、電荷:0 | |
| 原子炉や加速器等から作られる、ベータ壊変して陽子になる | ||
| 電磁波 | ガンマ線 | 光子、波長:10-11m以下 |
| 励起状態の原子核が励起エネルギー分のガンマ線を放出して基底状態になる | ||
| X線 | 光子、波長:10-12~10-8m | |
| 特別なベータ変換では、陽電子放出の代わりに原子核の内側の軌道の電子を吸収して | ||
| 外側の軌道の電子が内側の軌道に移り、軌道差のエネルギーのX線が放出される | ||
放射性変換:アルファ変換、電子/陽電子/X線を放出するベータ変換、ガンマ線放出
電離放射線:荷電粒子線、非荷電粒子線、3千兆ヘルツ以上の電磁波(ガンマ線、X線)
非電離放射線:3千兆ヘルツ以下の電磁波(紫外線の一部、可視光線、赤外線、マイクロ波、電波)
放射線検出器:霧箱によって荷電粒子(アルファ線、ベータ線、宇宙線)の飛跡を見ることができる
放射線測定器:GM管式(ベータ線)
シンチレーション式(ガンマ線、X線)測定器によってはアルファ線も測定可能
電離箱式(ガンマ線、X線)
電離放射線:荷電粒子線、非荷電粒子線、3千兆ヘルツ以上の電磁波(ガンマ線、X線)
非電離放射線:3千兆ヘルツ以下の電磁波(紫外線の一部、可視光線、赤外線、マイクロ波、電波)
放射線検出器:霧箱によって荷電粒子(アルファ線、ベータ線、宇宙線)の飛跡を見ることができる
放射線測定器:GM管式(ベータ線)
シンチレーション式(ガンマ線、X線)測定器によってはアルファ線も測定可能
電離箱式(ガンマ線、X線)
| 電磁波 | 波長 | 主な利用 |
|---|---|---|
| ガンマ線 | 10-10~10-12cm | 科学観測機器 |
| X線 | 10-7cm | 医療機器 |
| 紫外線 | 10-6cm | 殺菌灯 |
| 可視光線 | 10-5cm | 光学機器 |
| 赤外線 | 10-3cm | 赤外線ヒーター |
| サブミリ波 | 0.1cm | 光通信システム |
| 電波 | 102~104cm | 携帯電話・TV・ラジオ・飛行機の通信 |
放射線:天然放射性物質や人工放射性物質からの放射線、宇宙線
放射線の利用:X線撮影、CT検査、重イオンビーム、ガンマナイフ、PET(陽電子放出断層撮影)
ラジオアイソトープ(RI)= 原子炉内の中性子を材料に照射して作られる放射性物質
天然にも存在し、放射性同位元素とも呼ばれ、医療用のほかに、工業・農業分野でも使われている
核医学検査 = 放射線を放出するRIを含んだ薬を使って、ガンマカメラで体内の状態を調べる検査です
①安定な原子核に外から高エネルギー粒子を入射し、原子核反応が起こると放射性核になることがある
②安定な原子核に外から中性子を入射・吸収させると、放射性核ができる
③安定な原子核に高エネルギー陽子を当てて、中の中性子を弾き飛ばすと放射性核ができる
不安定な放射性核は放射線を放出して、静止質量エネルギーの低い原子核(安定核)に変わる
原子力エネルギー:ウラニウムやトリウムの核分裂の際の放出エネルギー … 原子力発電で利用中
核融合エネルギー:重水素や三重水素などの核融合の際の放出エネルギー
数百万~1千万eV:電子線(ベータ線)、陽子線、アルファ線、ガンマ線
1千億eV:宇宙線(ミュー粒子)、化学反応は数eVで放射線エネルギーの百万分の1
放射性変換前後の質量差:E=mc2 … これが放射線エネルギーが高い理由
核分裂の連鎖反応:ウラニウムが中性子を吸収して核分裂が起こり中性子を放出する
核燃料の燃焼制御:原子炉では中性子の減速材や中性子を吸収する制御棒が使われる
核融合の実用化:1億度位の超高温のプラズマをある時間維持し核融合の持続が必要
放射線の利用:X線撮影、CT検査、重イオンビーム、ガンマナイフ、PET(陽電子放出断層撮影)
ラジオアイソトープ(RI)= 原子炉内の中性子を材料に照射して作られる放射性物質
天然にも存在し、放射性同位元素とも呼ばれ、医療用のほかに、工業・農業分野でも使われている
核医学検査 = 放射線を放出するRIを含んだ薬を使って、ガンマカメラで体内の状態を調べる検査です
原子核内の核子の軌道運動→高エネルギー粒子を原子核に衝突させると、
高エネルギー粒子のエネルギーの大きさに応じて下記のいずれかが起こる
原子核の振動→原子核の回転→原子核反応→高温核の生成と核子の蒸発→
沢山の核子が蒸発、終には原子核は核子や小さな原子核にばらばらになる
高エネルギー粒子のエネルギーの大きさに応じて下記のいずれかが起こる
原子核の振動→原子核の回転→原子核反応→高温核の生成と核子の蒸発→
沢山の核子が蒸発、終には原子核は核子や小さな原子核にばらばらになる
①安定な原子核に外から高エネルギー粒子を入射し、原子核反応が起こると放射性核になることがある
②安定な原子核に外から中性子を入射・吸収させると、放射性核ができる
③安定な原子核に高エネルギー陽子を当てて、中の中性子を弾き飛ばすと放射性核ができる
不安定な放射性核は放射線を放出して、静止質量エネルギーの低い原子核(安定核)に変わる
|
宇宙線由来の放射線:中性子→大気中のN14→放射性同位体C14+H、C14+О2…→C14О2
炭素同位体年代測定:遺物や化石に含まれる炭素14(放射性同位体C14)の量を測定する↓放射性崩壊 (半減期5730±40年)→N14+e-+νe
炭素14の中性子1個が弱ボソンの作用で陽子に変わり、窒素14に変わる = β-崩壊
中性子中のdクォークが弱ボソンを放出してuクォークになる 弱ボソンはすぐにこわれて電子と反電子ニュートリノに変わる 炭素14=陽子6個+中性子8個 窒素14=陽子7個+中性子7個 |
原子力エネルギー:ウラニウムやトリウムの核分裂の際の放出エネルギー … 原子力発電で利用中
核融合エネルギー:重水素や三重水素などの核融合の際の放出エネルギー
数百万~1千万eV:電子線(ベータ線)、陽子線、アルファ線、ガンマ線
1千億eV:宇宙線(ミュー粒子)、化学反応は数eVで放射線エネルギーの百万分の1
放射性変換前後の質量差:E=mc2 … これが放射線エネルギーが高い理由
核分裂の連鎖反応:ウラニウムが中性子を吸収して核分裂が起こり中性子を放出する
核燃料の燃焼制御:原子炉では中性子の減速材や中性子を吸収する制御棒が使われる
核融合の実用化:1億度位の超高温のプラズマをある時間維持し核融合の持続が必要
|
中性子(点火剤)→U235核分裂→中性子+U238(天然核燃料)→U239→β変換→Np239→β変換→Pu239 →I131,Cs137,Sr90…,Xe133→β変換→Cs133+中性子→Cs134 Pu239は人工核燃料になるが、一部は中性子を吸収してPu240になり、一部は中性子により核分裂する 核分裂による静止質量エネルギーの変化はウラニウム核あたり0.01%、エネルギーにして2億電子ボルト 半減期が数万年以上の放射能をもつ長寿命核種MA(Np,Am,Cm)の群分離・核変換技術の開発が求められている 資源量の多いトリウムによるトリウム燃料サイクルは、MAの生成量が小さい利点があるが課題も多い |
|
500万eVの放射線の速さと透過する厚さ 1000万eVの放射線の防御 アルファ線 :光速の5%、 アルミホイル0.002cmで止まる 銅箔0.03mm 陽子線 :光速の10%、 アルミ板0.02cmで止まる 銅箔0.25mm ベータ線(電子):光速の99.5%、アルミ板1cmで止まる 銅板6mm ガンマ線(光子):光速、 アルミレンガ20cmで1/4に減少 銅ブロック10cmで1/10,15cmで2/100に減少 中性子線 :光速の4.67%、 数十cm~数mのコンクリートで減らす |
|
宇宙線 :ほぼ光速に近い速さ、 1000億eV、地下250m |
ガンマ線:物質中の電子に何回か衝突すると吸収されて消滅する(一部又は全部が電子のエネルギーになる)
光子は電子に衝突して、散乱、吸収、電子・陽電子対に変換される
中性子線:物質中の原子核に衝突して吸収されて消滅する
放射性物質は、壊変(崩壊)を繰り返し、最終的に安定した物質へ変化すると放射線を放出しなくなります
原子核の壊変には、規則性があり、放射能の量はある一定の時間が経過すると半分になり、更にその同じ
一定の時間が経過するとまたその半分になります … (1→1/2→1/4→1/8…)一定の時間:半減期は同じ
放射線の強度(ベクレル):放射性核数×変換率(%/年)、平均寿命=1/変換率、半減期=平均寿命の約70%
原子核の壊変には、規則性があり、放射能の量はある一定の時間が経過すると半分になり、更にその同じ
一定の時間が経過するとまたその半分になります … (1→1/2→1/4→1/8…)一定の時間:半減期は同じ
放射線の強度(ベクレル):放射性核数×変換率(%/年)、平均寿命=1/変換率、半減期=平均寿命の約70%
|
物理学的半減期:壊変によって、始めの原子核の数が半分になるまでの時間を半減期といいます 半減期は、放射性物質によって違い、数秒のものから100億年を超えるものまであります 生物学的半減期:体内に取り込まれた放射性物質の量が代謝や排泄により体の外へ排出されて半分になる までの時間 実効半減期 :物理学的半減期と生物学的半減期の両方を考慮したもの |
| 放射性物質 | 物理学的半減期 | 放射性物質 | 物理学的半減期 |
|---|---|---|---|
| クリプトン90 | 32.3秒 | クリプトン85 | 11 |
| キセノン138 | 14.1分 | トリチウム | 12.3 |
| フッ素18 | 109.8分 | ストロンチウム90 | 28.8 |
| ナトリウム24 | 15時間 | セシウム137 | 30.0 |
| ラドン222 | 3.8日 | ラジウム226 | 1600 |
| キセノン133 | 5.2日 | 炭素14 | 5700 |
| ヨウ素131 | 8.04日 | プルトニウム239 | 2.4万 |
| ストロンチウム89 | 50.5日 | ウラン235 | 7.0億 |
| ポロニウム210 | 138.4日 | カリウム40 | 13億 |
| セシウム134 | 2.1 | ウラン238 | 45億 |
| コバルト60 | 5.27 | トリウム232 | 141億 |
| 系列:放射性原子核から安定な原子核になるまで次々に核種が変化しながら壊変する | |||
| 非系列:系列を作らず放射性原子核から直接(1回の壊変で)安定な原子核になる | |||
|
ベクレル (Bq):1秒間に壊変(崩壊)する原子核の数で、放射能を表す単位、Bq/ℓ、Bq/kg シーベルト(Sv):体が受けた放射線による影響の度合いを表す単位、ミリSv、μSv グレイ (Gy):放射線のエネルギーが物質や人体の組織に吸収された量を表す単位、ナノGy、μGy |
※原子爆弾の放出したエネルギーの50%は爆風に、 35%は熱線に、15%は放射線となりました
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族→ 周期 |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | 1 H 水素 | 2 He ヘリウム | ||||||||||||||||
| 2 | 3 Li リチウム |
4 Be ベリリウム |
上段:原子番号(陽子数)、下段:日本名 中段:元素記号(文字色は常温の相) |
5 B ホウ素 |
6 C 炭素 |
7 N 窒素 |
8 O 酸素 |
9 F フッ素 |
10 Ne ネオン | |||||||||
| 3 | 11 Na ナトリウム |
12 Mg マグネシウム | 13 Al アルミニウム |
14 Si ケイ素 |
15 P リン |
16 S 硫黄 |
17 Cl 塩素 |
18 Ar アルゴン | ||||||||||
| 4 | 19 K カリウム |
20 Ca カルシウム |
21 Sc スカンジウム |
22 Ti チタン |
23 V バナジウム |
24 Cr クロム |
25 Mn マンガン |
26 Fe 鉄 |
27 Co コバルト |
28 Ni ニッケル |
29 Cu 銅 |
30 Zn 亜鉛 |
31 Ga ガリウム |
32 Ge ゲルマニウム |
33 As ヒ素 |
34 Se セレン |
35 Br 臭素 |
36 Kr クリプトン |
| 5 | 37 Rb ルビジウム |
38 Sr ストロンチウム |
39 Y イットリウム |
40 Zr ジルコニウム |
41 Nb ニオブ |
42 Mo モリブデン |
43 Tc テクネチウム |
44 Ru ルテニウム |
45 Rh ロジウム |
46 Pd パラジウム |
47 Ag 銀 |
48 Cd カドミウム |
49 In インジウム |
50 Sn スズ |
51 Sb アンチモン |
52 Te テルル |
53 I ヨウ素 |
54 Xe キセノン |
| 6 | 55 Cs セシウム |
56 Ba バリウム |
ランタ ノイド |
72 Hf ハフニウム |
73 Ta タンタル |
74 W タングステン |
75 Re レニウム |
76 Os オスミウム |
77 Ir イリジウム |
78 Pt 白金 |
79 Au 金 |
80 Hg 水銀 |
81 Tl タリウム |
82 Pb 鉛 |
83 Bi ビスマス |
84 Po ポロニウム |
85 At アスタチン |
86 Rn ラドン |
| 7 | 87 Fr フランシウム |
88 Ra ラジウム |
アクチ ノイド |
104 Rf ラザホージウム |
105 Db ドブニウム |
106 Sg シーボーギウム |
107 Bh ボーリウム |
108 Hs ハッシウム |
109 Mt マイトネリウム |
110 Ds ダームスタチウム |
111 Rg レントゲニウム |
112 Cn コペルニシウム |
113 Nh ニホニウム |
114 Fl フレロビウム |
115 Mc モスコビウム |
116 Lv リバモリウム |
117 Ts テネシン |
118 Og オガネソン |
上記周期表は「長周期型周期表」と呼ばれるもので、「ランタノイド(57番〜71番元素)」
や「アクチノイド(89番〜103番元素)」といった元素群が、表の下側に置かれています
一方、超長周期型の周期表では、ランタノイドやアクチノイドも一つの表の中におさめます
つまり、長周期型と超長周期型は、元素の配置の仕方がちがうだけで、内容は同じものです
や「アクチノイド(89番〜103番元素)」といった元素群が、表の下側に置かれています
一方、超長周期型の周期表では、ランタノイドやアクチノイドも一つの表の中におさめます
つまり、長周期型と超長周期型は、元素の配置の仕方がちがうだけで、内容は同じものです
| ランタ ノイド |
57 La ランタン |
58 Ce セリウム |
59 Pr プラセオジム |
60 Nd ネオジム |
61 Pm プロメチウム |
62 Sm サマリウム |
63 Eu ユウロピウム |
64 Gd ガドリニウム |
65 Tb テルビウム |
66 Dy ジスプロシウム |
67 Ho ホルミウム |
68 Er エルビウム |
69 Tm ツリウム |
70 Yb イッテルビウム |
71 Lu ルテチウム |
| アクチ ノイド |
89 Ac アクチニウム |
90 Th トリウム |
91 Pa プロトアクチニウム |
92 U ウラン |
93 Np ネプツニウム |
94 Pu プルトニウム |
95 Am アメリシウム |
96 Cm キュリウム |
97 Bk バークリウム |
98 Cf カリホルニウム |
99 Es アインスタイニウム |
100 Fm フェルミウム |
101 Md メンデレビウム |
102 No ノーベリウム |
103 Lr ローレンシウム |
背景の色=非金属、アルカリ金属、アルカリ土類金属、遷移金属、ハロゲン、貴ガス、典型金属
金属元素:金属元素、非金属元素:金属元素以外、半金属元素:金属と非金属との境界付近の元素(両方の性質)
遷移元素(横の類似性):3~12族、3族のうち原子番号=57~70と原子番号=89~102は内部遷移元素
典型元素(縦の類似性):遷移元素以外、典型元素には非金属元素と金属元素がある、テネシンも典型元素に含む
内部遷移元素:原子番号=57~70:ランタノイド(La~Yb)、原子番号=89~102:アクチノイド(Ac~No)
希土類元素(17元素):Scスカンジウム,Yイットリウム,ランタノイド=(「ランタン」+「もどき」)
貴ガスは量的に少ないので希ガスとも言われる化合反応を起こしにくい不活性ガス(最外殻までの電子が満杯状態)
2005年に英語表記がrare gasからnoble gasに改められ,日本語での表記も希ガスから貴ガスへと変更になりました
令和3年度の教科書より、日本化学会の提言も踏まえて高貴なガスという意味から貴ガスと表記を変更しています
化学反応しやすい:電子が満杯+1個余計(Na+)、電子が満杯-1個少ない(Cl-)=化学反応を起こしてNaClになる
第12族から第16族は先頭元素名で呼ばれる(亜鉛族,ホウ素族,炭素族,窒素族,酸素族)
ニクトゲン:15族に位置する5つの元素(N,P,As,Sb,Bi),カルコゲン:16族に位置する5つの元素(O,S,Se,Te,Po)
人工元素:天然に存在する元素は原則、原子番号92Uウランまでですが、原子番号92までのうち4つの例外元素
=43Tcテクネチウム,61Pmプロメチウム,85Atアスタチン,87Frフランシウム(同位体)および原子番号が93以上の
超ウラン元素(アクチノイドの一部93~103,104-118の24個),いずれも放射性元素
|
殻 ---spdf軌道---
K 1s L 2s 2p M 3s 3p 3d N 4s 4p 4d 4f O 5s 5p 5d 5f P 6s 6p 6d 6f Q 7s 7p 7d 7f 2 6 10 14 |
電子殻は内側から、K殻、L殻、M殻、N殻…です 各電子殻に入ることのできる電子の数は限りがあって、 K殻に2個、L殻に8個、M殻に18個、N殻に32個となります 電子が電子殻に入るとき、その入り方には規則性(電子配置)がある 規則性①‥電子は普通内側にある電子殻(K殻)から順に入る 内側から入った電子が電子殻の収容できる数を超えるとその外側の電子殻に入る 規則性②‥最外殻電子の数が8個を超えてはいけない(ただし、Pdは例外) 原子は安定な電子殻が多い方を目指す(Ca20の場合、K2,L8,M10でなく、K2,L8,M8,N2) 遷移元素はこの規則性に従わない(後述の例外1,例外2,例外3) |
殻 K L L M M N M N O N O P N O P Q O P Q P Q Q
軌道1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s→4f→5d→6p→7s→5f→6d→7p→6f→7d→7f
(E)1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p<6f<7d<7f
という順で詰まっていきます(銅などいくつかの例外もある)
○主量子数:n = 1,2,3,…,7 (正の整数) = 電子殻:K,L,M,N,…殻
○主量子数nと方位量子数l(エル)との関係…0≦l≦n-1
○方位量子数l(エル)と磁気量子数mlとの関係…-l≦ml≦l
エネルギー準位(E)は、通常、主量子数(n)が大きくなるほど高く、主量子数(n)が同じ値の場合には、
方位量子数(l:エル)の値が大きくなるほど高いが、n≧3の場合は、高低の逆転が生じる(4s<3d)
このように見ると、M殻の3d軌道の前にN殻の4s軌道が詰まるなど「K殻から順に」のルールが崩れています
実はこれこそが「遷移元素」が存在する理由です
電子軌道は、エネルギーの低い順に収容される(4s<3d)
例として原子番号21、電子数21のスカンジウムを見ていきます
カルシウムは電子数20ですから、電子1個を残して全てカルシウムと同じように詰まります
カルシウムはK殻に2個、L殻に8個、M殻に8個入ると、あと10個の電子がM殻に入れるのですが、
残り2個の電子は、M殻より軌道エネルギーの低いN殻に先に入ります(4s<3d)
(Ca20の場合、K2,L8,M10でなく、K2,L8,M8,N2)
K L L M M N
20Ca:1s2→2s2→2p6→3s2→3p6→4s2
電子数 2 4 10 12 18 20
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期4 | N殻 | ↑ | ↓ | … | |||||||||||||||||||||||
| : | |||||||||||||||||||||||||||
| ↑ | ↓ |
| ↑ | ↑ | ↑ |
K L L M M N M
21Sc:1s2→2s2→2p6→3s2→3p6→4s2→3d1
電子数 2 4 10 12 18 20 21
この先最外殻電子は4s軌道の2個のまま、3d軌道に入っていくことになり、これが「遷移元素」が生じる原因です
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | |||||||||||||||||
| 周期4 | N殻 | ↑ | ↓ | … | |||||||||||||||||||||||
| : | |||||||||||||||||||||||||||
亜鉛族元素:第12族元素は、d軌道が閉殻状態ゆえ典型元素的性質を持つため、以前は「典型元素」に分類され
ていましたが、IUPACの最近の勧告にあわせて、日本も2022年度からは「遷移元素」に含めるとしています
従来の周期表の中には、(La~Lu)及び((Ac~Lr)の各15元素を「内部遷移元素」としているものもありますが、
電子配置からするとLu及びLrは「内部遷移元素」でなく「遷移元素」です
本来、内部遷移元素は(n-2)f1-14の電子を持ち、各シリーズ14個の元素からなることが特長です
ランタノイド(La~Lu)15個のうちLuを除外した(La~Yb)が内部遷移元素14個、Luは遷移元素
(La~Yb)+(Lu~Hg):(14+10)元素=4f+5d
アクチノイド(Ac~Lr)15個のうちLrを除外した(Ac~No)が内部遷移元素14個、Lrは遷移元素
(Ac~No)+(Lr~Cn):(14+10)元素=5f+6d
1番外側の電子殻に収容されている電子のことを最外殻電子といいます
貴ガスの最外殻電子はヘリウムだけ2個で、他の貴ガスはすべて最外殻電子は8個で安定な電子配置をしています
このように最大数の電子が収容された電子殻を閉殻といいます
化学結合や化学的性質に関与する電子のことを価電子といいます
最外殻電子がちょうどその電子殻の最大収容数の場合、または最外殻電子が8個の場合、価電子の数は0とする
貴ガスの場合は最外殻までの電子が満杯状態で、化学反応をそもそも起こさないので、価電子の数はゼロです
価電子の定義は曖昧です(貴ガスは反応性が低いから価電子数はすべて0としますと言う程度の定義です!)
同一元素の原子はその原子核に必ず同数の陽子を持っているが、中性子数の異なる原子核(核種)を同位体と呼ぶ
同位体は陽子と軌道電子の数が等しいため化学的性質はほぼ等しいが、物理的性質は異なる
同位体のうち放射性を有するものを放射性同位体、放射性を有しないものを安定同位体と呼ぶ
| 族→ 周期 |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | 1 水素 1766 | 2 ヘリウム 1868 | ||||||||||||||||
| 2 | 3 リチウム 1817 |
4 ベリリウム 1798 |
上段:原子番号、中段:日本名、下段:発見年 | 5 ホウ素 1808 |
6 炭素 古代 |
7 窒素 1772 |
8 酸素 1774 |
9 フッ素 1886 |
10 ネオン 1898 | |||||||||
| 3 | 11 ナトリウム 1807 |
12 マグネシウム 1755 | 13 アルミニウム 1825 |
14 ケイ素 1823 |
15 リン 1669 |
16 硫黄 古代 |
17 塩素 1774 |
18 アルゴン 1894 | ||||||||||
| 4 | 19 カリウム 1807 |
20 カルシウム 1808 |
21 スカンジウム 1879 |
22 チタン 1795 |
23 バナジウム 1801 |
24 クロム 1797 |
25 マンガン 1774 |
26 鉄 古代 |
27 コバルト 1737 |
28 ニッケル 1751 |
29 銅 古代 |
30 亜鉛 古代 |
31 ガリウム 1875 |
32 ゲルマニウム 1886 |
33 ヒ素 1250 |
34 セレン 1817 |
35 臭素 1826 |
36 クリプトン 1898 |
| 5 | 37 ルビジウム 1860 |
38 ストロンチウム 1793 |
39 イットリウム 1794 |
40 ジルコニウム 1789 |
41 ニオブ 1846 |
42 モリブデン 1778 |
43 テクネチウム 1937 |
44 ルテニウム 1844 |
45 ロジウム 1803 |
46 パラジウム 1803 |
47 銀 古代 |
48 カドミウム 1817 |
49 インジウム 1863 |
50 スズ 古代 |
51 アンチモン 1450 |
52 テルル 1782 |
53 ヨウ素 1811 |
54 キセノン 1898 |
| 6 | 55 セシウム 1860 |
56 バリウム 1774 |
ランタ ノイド |
72 ハフニウム 1923 |
73 タンタル 1802 |
74 タングステン 1783 |
75 レニウム 1925 |
76 オスミウム 1803 |
77 イリジウム 1803 |
78 白金 1741 |
79 金 古代 |
80 水銀 古代 |
81 タリウム 1860 |
82 鉛 古代 |
83 ビスマス 1753 |
84 ポロニウム 1898 |
85 アスタチン 1940 |
86 ラドン 1898 |
| 7 | 87 フランシウム 1939 |
88 ラジウム 1898 |
アクチ ノイド |
104 ラザホージウム 1964 |
105 ドブニウム 1970 |
106 シーボーギウム 1974 |
107 ボーリウム 1976 |
108 ハッシウム 1984 |
109 マイトネリウム 1982 |
110 ダームスタチウム 1994 |
111 レントゲニウム 1994 |
112 コペルニシウム 1996 |
113 ニホニウム 2004 |
114 フレロビウム 1999 |
115 モスコビウム 2004 |
116 リバモリウム 2000 |
117 テネシン 2009 |
118 オガネソン 2003 |
| ランタ ノイド |
57 ランタン 1839 |
58 セリウム 1803 |
59 プラセオジム 1885 |
60 ネオジム 1885 |
61 プロメチウム 1945 |
62 サマリウム 1879 |
63 ユウロピウム 1901 |
64 ガドリニウム 1880 |
65 テルビウム 1843 |
66 ジスプロシウム 1886 |
67 ホルミウム 1879 |
68 エルビウム 1843 |
69 ツリウム 1879 |
70 イッテルビウム 1878 |
71 ルテチウム 1907 |
| アクチ ノイド |
89 アクチニウム 1899 |
90 トリウム 1828 |
91 プロトアクチニウム 1917 |
92 ウラン 1789 |
93 ネプツニウム 1940 |
94 プルトニウム 1941 |
95 アメリシウム 1945 |
96 キュリウム 1944 |
97 バークリウム 1949 |
98 カリホルニウム 1950 |
99 アインスタイニウム 1952 |
100 フェルミウム 1953 |
101 メンデレビウム 1955 |
102 ノーベリウム 1958 |
103 ローレンシウム 1961 |
元素数 = 10個、 1個、 1個、 1個、 21個、 49個、 30個、 5個
地表露出:有用資源の採掘
熱分解・電気分解:化合物を単体に分解
分光器:分光分析、スペクトル分析
周期律の発見:三つ組元素、未知元素の予言(周期表の空欄)
放射線:放射性元素の発見
加速器:原子核反応、人工元素、現代の錬金術
| 族→ 周期 |
Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | ||
| 1 | 1 H 水素 | 2 He ヘリウム | ||||||||
| 2 | 3 Li リチウム |
4 Be ベリリウム |
上段:原子番号(陽子数) 中段:元素記号 |
5 B ホウ素 |
6 C 炭素 |
7 N 窒素 |
8 O 酸素 |
9 F フッ素 |
10 Ne ネオン | |
| 3 | 11 Na ナトリウム |
12 Mg マグネシウム |
(文字色は常温の相) 下段:日本名 |
13 Al アルミニウム |
14 Si ケイ素 |
15 P リン |
16 S 硫黄 |
17 Cl 塩素 |
18 Ar アルゴン | |
| 4 | 19 K カリウム |
20 Ca カルシウム |
21~30 Sc~Zn スカンジウム~亜鉛 |
31 Ga ガリウム |
32 Ge ゲルマニウム |
33 As ヒ素 |
34 Se セレン |
35 Br 臭素 |
36 Kr クリプトン | |
| 5 | 37 Rb ルビジウム |
38 Sr ストロンチウム |
39~48 Y~Cd イットリウム~カドミウム |
49 In インジウム |
50 Sn スズ |
51 Sb アンチモン |
52 Te テルル |
53 I ヨウ素 |
54 Xe キセノン | |
| 6 | 55 Cs セシウム |
56 Ba バリウム |
57~70 La~Yb ランタン~イッテルビウム |
71~80 Lu~Hg ルテチウム~水銀 |
81 Tl タリウム |
82 Pb 鉛 |
83 Bi ビスマス |
84 Po ポロニウム |
85 At アスタチン |
86 Rn ラドン |
| 7 | 87 Fr フランシウム |
88 Ra ラジウム |
89~102 Ac~No アクチニウム~ノーベリウム |
103~112 Lr~Cn ローレンシウム~コペルニシウム |
113 Nh ニホニウム |
114 Fl フレロビウム |
115 Mc モスコビウム |
116 Lv リバモリウム |
117 Ts テネシン |
118 Og オガネソン |
最外殻電子の数が同じ元素は同じ族にまとめた周期表
第4軌道以降は、p軌道の前の隙間(d軌道やf軌道)に電子が入り込み、
元素はどれも同じような性質を示す
メンデレーエフの第二の周期表をベースに貴ガスやLn(57-71)An(89-103)を追加
亜族を追加(A&B)した短周期型周期表
IB,ⅡB,ⅢA–ⅦA,O族をまるごとⅧ族の右に引越した短周期型周期表
亜族問題の解決とブロック(spdf)の分類を同時に達成
族の名称を1–18族と呼ぶことに改めた長周期型周期表
1–18族(縦の同族元素のグループ)
短周期型周期表の改良版
左端のⅠ-Ⅱと右端のⅢ-Oとの間のⅢ-Ⅷ,Ⅰ-Ⅱ族(f軌道とd軌道)の族名を消去
f軌道とd軌道のブロックのグループ化(縦の同族元素のグループの例外)、遷移元素
超長周期型周期表
第4軌道以降は、p軌道の前の隙間(d軌道やf軌道)に電子が入り込み、
元素はどれも同じような性質を示す
メンデレーエフの第二の周期表をベースに貴ガスやLn(57-71)An(89-103)を追加
亜族を追加(A&B)した短周期型周期表
| 族→ 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | O | Ⅷ | Ⅷ | Ⅷ | |||||||||||
| A | B | A | B | A | B | A | B | A | B | A | B | A | B | |||||||||
| 1 | H | He | ||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||
| 4 | K | Cu | Ca | Zn | Sc | Ga | Ti | Ge | V | As | Cr | Se | Mn | Br | Kr | Fe | Co | Ni | ||||
| 5 | Rb | Ag | Sr | Cd | Y | In | Sn | Nb | Sb | Mo | Te | Tc | I | Xe | Ru | Rh | Pd | |||||
| 6 | Cs | Au | Ba | Hg | La~Lu | Tl | Hf | Pb | Ta | Bi | W | Po | Re | At | Rn | Os | Ir | Pt | ||||
| 7 | Fr | Rg | Ra | Cn | Ac~Lr | Nh | Rf | Fl | Db | Mc | Sg | Lv | Bh | Ts | Og | Hs | Mt | Ds | ||||
亜族問題の解決とブロック(spdf)の分類を同時に達成
| 族→ 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | Ⅷ | Ⅷ | Ⅷ | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | O |
| 1 | H | He | ||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| 4 | K | Ca | Sc | Ti | Ⅴ | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| 6 | Cs | Ba | La~Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac~Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
1–18族(縦の同族元素のグループ)
| 価電子数 | 1 | 2 | 1か2 | 3 | 4 | 5 | 6 | 7 | 0 | |||||||||
| 族→ 周期 |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | H | He | ||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| 4 | K | Ca | Sc | Ti | Ⅴ | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| 6 | Cs | Ba | La~Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac~Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
左端のⅠ-Ⅱと右端のⅢ-Oとの間のⅢ-Ⅷ,Ⅰ-Ⅱ族(f軌道とd軌道)の族名を消去
f軌道とd軌道のブロックのグループ化(縦の同族元素のグループの例外)、遷移元素
| 族→ 周期 |
Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | ||
| 1 | 2 | 3 | 3-12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | H | He | ||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||
| 4 | K | Ca | Sc~Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y~Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | La~Yb | Lu~Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac~No | Lr~Cn | Nh | Fl | Mc | Lv | Ts | Og |
| A(2) | 内部遷移元素C(14) | 遷移元素B(10) | 典型元素A(6) | |||||||||||||||||||||||||||||
| 族→ 周期 | ⅠA | ⅡA | ⅠC~ⅩⅣC | ⅠB~ⅩB | ⅢA~ⅧA | |||||||||||||||||||||||||||
| 1 | 2 | 3 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | Ⅴ | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
|
左記の表から特定の元素の電子数と
原子番号が求められます 周期 元素数 軌道 1 2 1s 2 8 2s 2p 3 8 3s 3p 4 18 4s 3d 4p 5 18 5s 4d 5p 6 32 6s 4f 5d 6p 7 32 7s 5f 6d 7p abc=電子殻a,電子軌道bの電子数がc個 (a:1~7,b:spdf,c:1~14) 電子殻a=1~7:K~Q、 電子軌道bの軌道数=s:1個,p:3個,d:5個,f:7個 軌道電子数最大 1x2 ,3x2 ,5x2 ,7x2 軌道電子数最大 s:2 ,p:6 ,d:10 ,f:14 例:34Seセレン 周期1:1s2 周期2:2s2,2p6 周期3:3s2,3p6 周期4:4s2,3d10,4p4 cの合計=1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p4 =34 よって、セレンの電子数=34:原子番号 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| TOP|貴ガスの電子配置|TOP | |||||||
|
◆引用の明示:Wikipedia◆
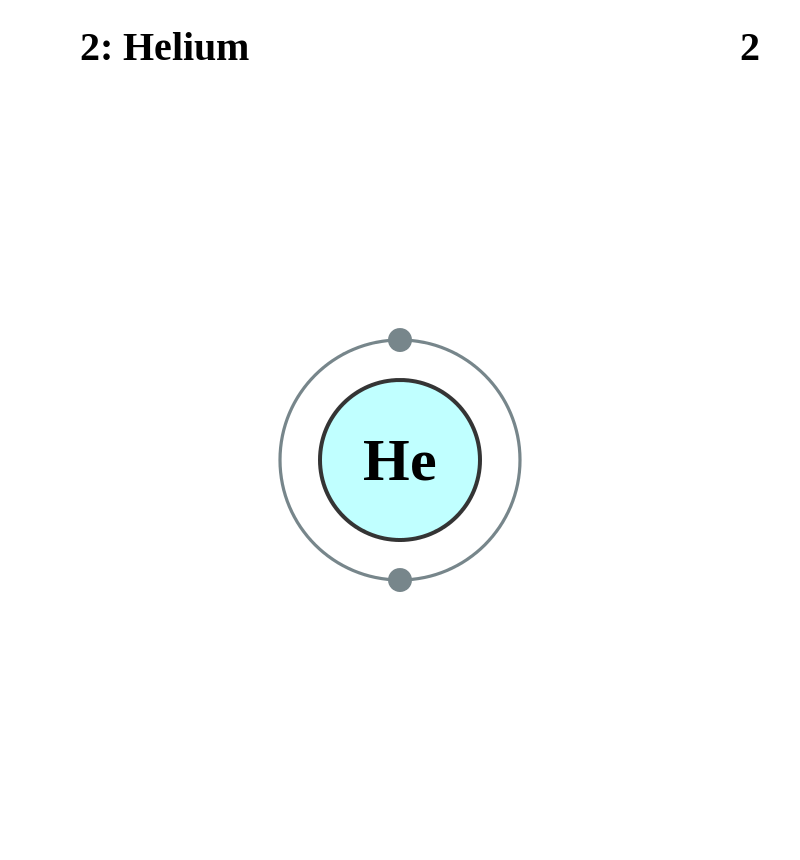
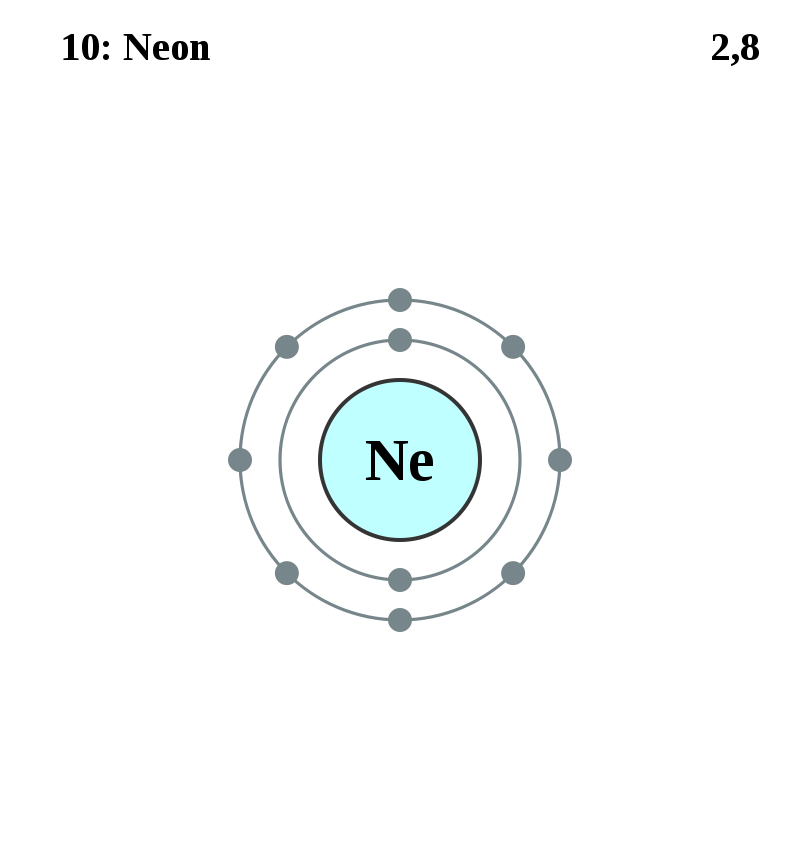
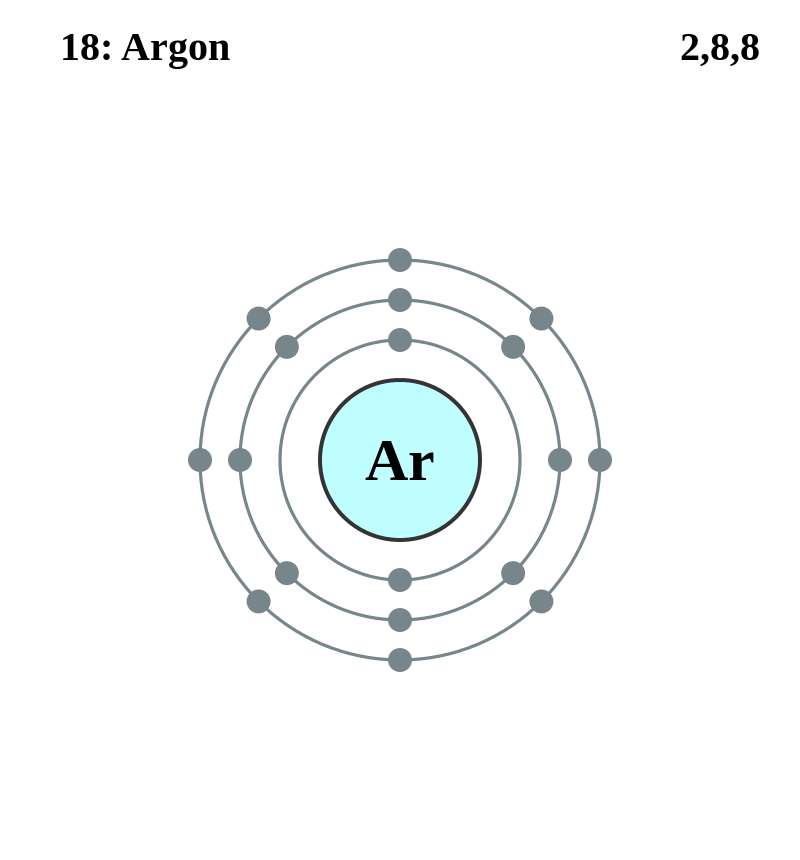
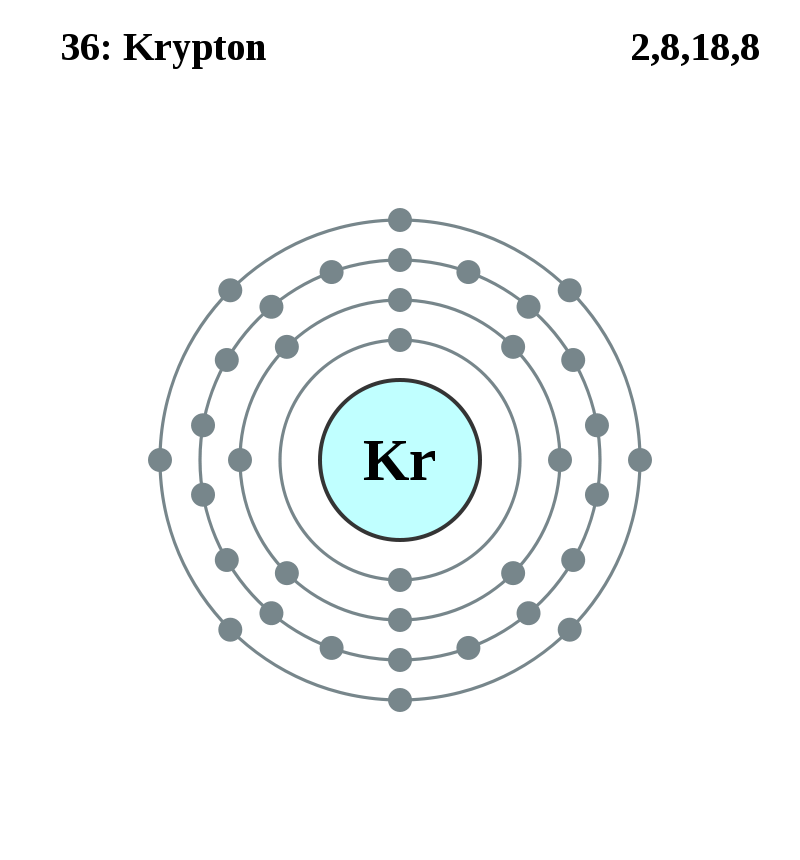
2=2 2+8=10 2+8+8=18 2+8+18+8=36
| |||||||
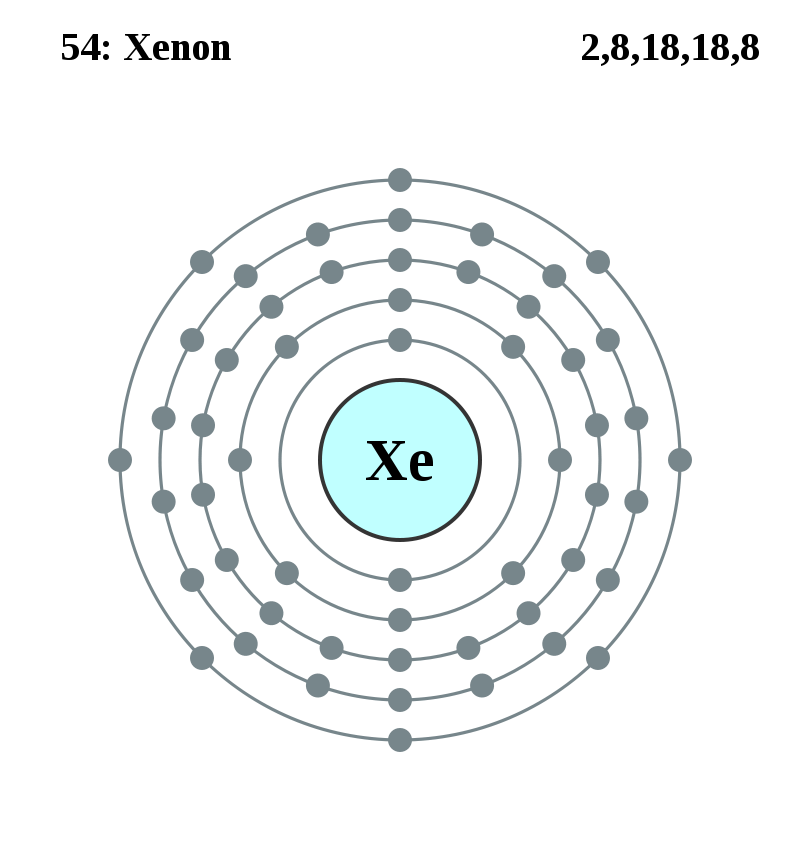
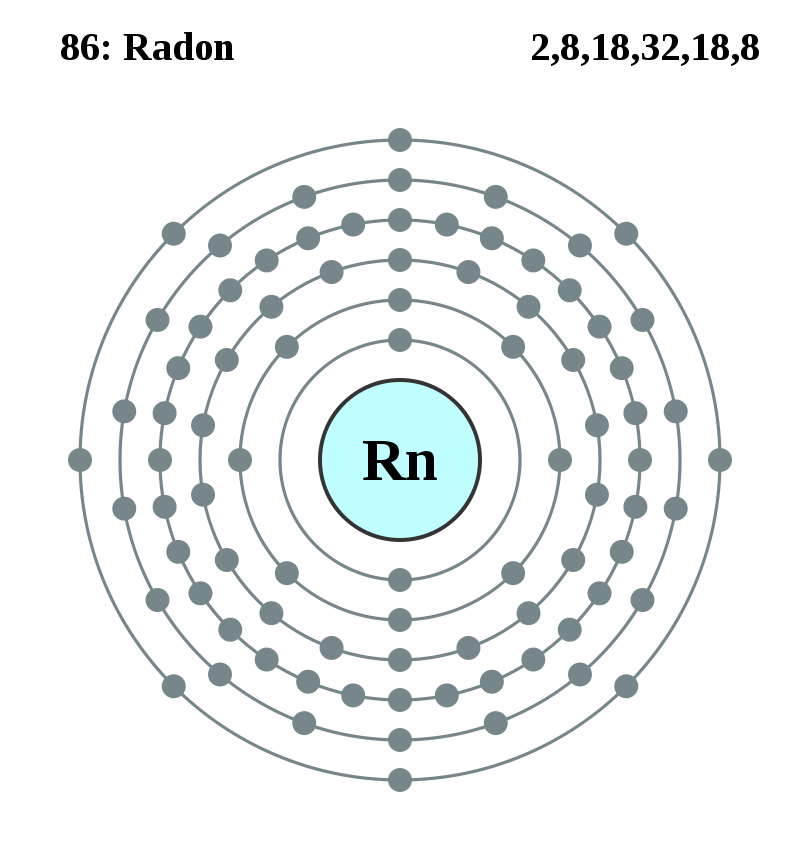
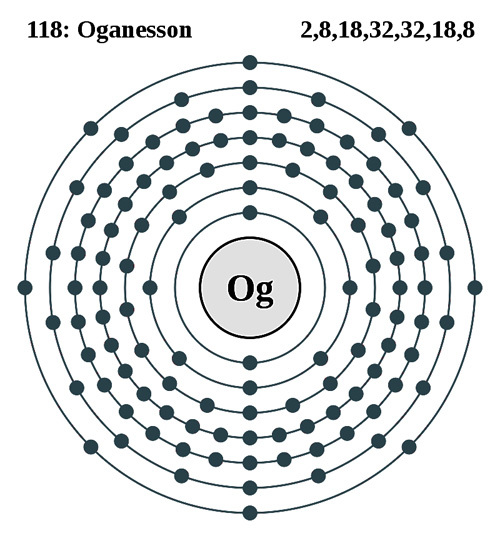
2+8+18+18+8=54 2+8+18+32+18+8=86 2+8+18+32+32+18+8=118
| |||||||
|
電子が軌道に入るときは、次の規則がある ①構成原理 :エネルギーの低い軌道から順に入っていく (例外あり) ②パウリの排他律:1つの軌道には電子が2個まで入ることができる(スピン= +1/2,-1/2) ③フントの規則 :複数の軌道があるときは電子はできるだけ別々の軌道にスピンの向きを揃えて入っていく 電子軌道bの軌道数=s:1個,p:3個,d:5個,f:7個 軌道電子数最大 1x2 ,3x2 ,5x2 ,7x2 | |||||||
|
最外殻電子数:1個~8個 最外殻電子数が8個の場合が貴ガス・不活性ガス 以下は、原子番号118のOgオガネソンの電子配置です ← [周期表の仕組み]の表のab行から後記(1) p軌道の前の隙間d軌道やf軌道に電子が入り込み:低いエネルギ―軌道 1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6,6s2,4f14,5d10,6p6,7s2,5f14,6d10,7p6 … (1) 1 2 3 4 5 6 7 ← 周期1~7 abc=電子殻a,電子軌道bの電子数がc個(a:1~7,b:spdf,c:1~14) 電子殻a=1~7:K~Q、軌道電子数最大=s:2,p:6,d:10,f:14、前記(1)を電子殻aで並べ直すと次行 1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6,4d10,4f14,5s2,5p6,5d10,5f14,6s2,6p6,6d10,7s2,7p6 K L M N O P Q ← 電子殻K~Q オガネソン=原子核に近い内側からK殻~Q殻=軌道殻7 電子配置 :K殻,L殻,M殻,N殻,O殻,P殻,Q殻 主量子数 : 1, 2, 3, 4, 5, 6, 7 電子収容数: 2, 8, 18, 32, 32, 18, 8 Σc 軌道の数 : 1, 4, 9, 16, 16, 9, 4 電子収容数/2 ●電子の数=2+8+18+32+32+18+8=118:オガネソンの原子番号 電子殻K~Q=K L M N O P Q ●元素の数=2+8+8+18+18+32+32=118:オガネソンの原子番号 周期1~7=1 2 3 4 5 6 7 | |||||||
|
ヘリウム=2 2 1s2
ネオン=2,8 10 1s2,2s2,2p6 アルゴン=2,8,8 18 1s2,2s2,2p6,3s2,3p6 クリプトン=2,8,18,8 36 1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6 キセノン=2,8,18,18,8 54 1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6,4d10 ,5s2,5p6 ラドン=2,8,18,32,18,8 86 1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6,4d10,4f14,5s2,5p6,5d10 ,6s2,6p6 オガネソン=2,8,18,32,32,18,8 118 1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6,4d10,4f14,5s2,5p6,5d10,5f14,6s2,6p6,6d10,7s2,7p6 電子殻K~Q=K L M N O P Q K L M N O P Q | |||||||
|
ヘリウム=2 2 1s2
ネオン=2,8 10 1s2,2s2,2p6 アルゴン=2,8,8 18 1s2,2s2,2p6,3s2,3p6 クリプトン=2,8,8,18 36 1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6 キセノン=2,8,8,18,18 54 1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6 ラドン=2,8,8,18,18,32 86 1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6,6s2,4f14,5d10,6p6 オガネソン=2,8,8,18,18,32,32 118 1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6,6s2,4f14,5d10,6p6,7s2,5f14,6d10,7p6 周期1~7=1 2 3 4 5 6 7 1 2 3 4 5 6 7 |
|||||||
| 最大電子数(殻) | 2 | 8 | 18 | 32 | 32 | 18 | 8 | 本来は | 例 外 | ||||||||||||||||
| 最大電子数(副殻) | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 14 | 2 | 6 | 10 | 14 | 2 | 6 | 10 | 2 | 6 | 1 | |||||
| 族 | 元素記号 | 元素名 | 原子 番号 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | 2 | ||
| K | L | M | N | O | P | Q | 3 | ||||||||||||||||||
| 第1周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | H | 水素 | 1 | 1 | |||||||||||||||||||||
| 18 | He | ヘリウム | 2 | 2 | |||||||||||||||||||||
| 第2周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | Li | リチウム | 3 | 2 | 1 | ||||||||||||||||||||
| 2 | Be | ベリリウム | 4 | 2 | 2 | ||||||||||||||||||||
| 13 | B | ホウ素 | 5 | 2 | 2 | 1 | |||||||||||||||||||
| 14 | C | 炭素 | 6 | 2 | 2 | 2 | |||||||||||||||||||
| 15 | N | 窒素 | 7 | 2 | 2 | 3 | |||||||||||||||||||
| 16 | O | 酸素 | 8 | 2 | 2 | 4 | |||||||||||||||||||
| 17 | F | フッ素 | 9 | 2 | 2 | 5 | |||||||||||||||||||
| 18 | Ne | ネオン | 10 | 2 | 2 | 6 | |||||||||||||||||||
| 第3周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | Na | ナトリウム | 11 | 10 1s … 2p ネオン核 [Ne] | 1 | ||||||||||||||||||||
| 2 | Mg | マグネシウム | 12 | 2 | |||||||||||||||||||||
| 13 | Al | アルミニウム | 13 | 2 | 1 | ||||||||||||||||||||
| 14 | Si | ケイ素 | 14 | 2 | 2 | ||||||||||||||||||||
| 15 | P | リン | 15 | 2 | 3 | ||||||||||||||||||||
| 16 | S | 硫黄 | 16 | 2 | 4 | ||||||||||||||||||||
| 17 | Cl | 塩素 | 17 | 2 | 5 | ||||||||||||||||||||
| 18 | Ar | アルゴン | 18 | 2 | 6 | ||||||||||||||||||||
| 第4周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | K | カリウム | 19 | 18 1s … 3p アルゴン核 [Ar] | 1 | ||||||||||||||||||||
| 2 | Ca | カルシウム | 20 | 2 | |||||||||||||||||||||
| 3 | Sc | スカンジウム | 21 | 1 | 2 | ||||||||||||||||||||
| 4 | Ti | チタン | 22 | 2 | 2 | ||||||||||||||||||||
| 5 | V | バナジウム | 23 | 3 | 2 | ||||||||||||||||||||
| 6 | Cr | クロム | 24 | 5 | 1 | 4 | 2 | 1 | |||||||||||||||||
| 7 | Mn | マンガン | 25 | 5 | 2 | ||||||||||||||||||||
| 8 | Fe | 鉄 | 26 | 6 | 2 | ||||||||||||||||||||
| 9 | Co | コバルト | 27 | 7 | 2 | ||||||||||||||||||||
| 10 | Ni | ニッケル | 28 | 8 | 2 | ||||||||||||||||||||
| 11 | Cu | 銅 | 29 | 10 | 1 | 9 | 2 | 1 | |||||||||||||||||
| 12 | Zn | 亜鉛 | 30 | 10 | 2 | ||||||||||||||||||||
| 13 | Ga | ガリウム | 31 | 10 | 2 | 1 | |||||||||||||||||||
| 14 | Ge | ゲルマニウム | 32 | 10 | 2 | 2 | |||||||||||||||||||
| 15 | As | ヒ素" | 33 | 10 | 2 | 3 | |||||||||||||||||||
| 16 | Se | セレン | 34 | 10 | 2 | 4 | |||||||||||||||||||
| 17 | Br | 臭素 | 35 | 10 | 2 | 5 | |||||||||||||||||||
| 18 | Kr | クリプトン | 36 | 10 | 2 | 6 | |||||||||||||||||||
| 第5周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | Rb | ルビジウム | 37 | 36 1s … 4p クリプトン核 [Kr] | 1 | ||||||||||||||||||||
| 2 | Sr | ストロンチウム | 38 | 2 | |||||||||||||||||||||
| 3 | Y | イットリウム | 39 | 1 | 2 | ||||||||||||||||||||
| 4 | Zr | ジルコニウム | 40 | 2 | 2 | ||||||||||||||||||||
| 5 | Nb | ニオブ" | 41 | 4 | 1 | 3 | 2 | 1 | |||||||||||||||||
| 6 | Mo | モリブデン | 42 | 5 | 1 | 4 | 2 | 1 | |||||||||||||||||
| 7 | Tc | テクネチウム | 43 | 5 | 2 | ||||||||||||||||||||
| 8 | Ru | ルテニウム | 44 | 7 | 1 | 6 | 2 | 1 | |||||||||||||||||
| 9 | Rh | ロジウム | 45 | 8 | 1 | 7 | 2 | 1 | |||||||||||||||||
| 10 | Pd | パラジウム | 46 | 10 | 8 | 2 | 1 | ||||||||||||||||||
| 11 | Ag | 銀 | 47 | 10 | 1 | 9 | 2 | 1 | |||||||||||||||||
| 12 | Cd | カドミウム | 48 | 10 | 2 | ||||||||||||||||||||
| 13 | In | インジウム | 49 | 10 | 2 | 1 | |||||||||||||||||||
| 14 | Sn | スズ | 50 | 10 | 2 | 2 | |||||||||||||||||||
| 15 | Sb | アンチモン | 51 | 10 | 2 | 3 | |||||||||||||||||||
| 16 | Te | テルル | 52 | 10 | 2 | 4 | |||||||||||||||||||
| 17 | I | ヨウ素" | 53 | 10 | 2 | 5 | |||||||||||||||||||
| 18 | Xe | キセノン | 54 | 10 | 2 | 6 | |||||||||||||||||||
| 第6周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | Cs | セシウム | 55 | 54=68-14 1s … 5p-(4f) キセノン核 [Xe] | 1 | ||||||||||||||||||||
| 2 | Ba | バリウム | 56 | 2 | |||||||||||||||||||||
| 3 | La | ランタン | 57 | 1 | 2 | 1 | 0 | 2 | |||||||||||||||||
| 3 | Ce | セリウム | 58 | 46=68-(14+2+6) 1s … 5p-(4f,5s,5p) キセノン核 [Xe] | 1 | 2 | 6 | 1 | 2 | 2 | 0 | 2 | |||||||||||||
| 3 | Pr | プラセオジム | 59 | 3 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Nd | ネオジム | 60 | 4 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Pm | プロメチウム | 61 | 5 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Sm | サマリウム | 62 | 6 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Eu | ユウロピウム | 63 | 7 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Gd | ガドリニウム | 64 | 7 | 2 | 6 | 1 | 2 | 8 | 0 | 2 | ||||||||||||||
| 3 | Tb | テルビウム | 65 | 9 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Dy | ジスプロシウム | 66 | 10 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Ho | ホルミウム | 67 | 11 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Er | エルビウム | 68 | 12 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Tm | ツリウム | 69 | 13 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Yb | イッテルビウム | 70 | 14 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Lu | ルテチウム | 71 | 68 1s … 5p キセノン核 [Xe] | 1 | 2 | |||||||||||||||||||
| 4 | Hf | ハフニウム | 72 | 2 | 2 | ||||||||||||||||||||
| 5 | Ta | タンタル | 73 | 3 | 2 | ||||||||||||||||||||
| 6 | W | タングステン | 74 | 4 | 2 | ||||||||||||||||||||
| 7 | Re | レニウム | 75 | 5 | 2 | ||||||||||||||||||||
| 8 | Os | オスミウム | 76 | 6 | 2 | ||||||||||||||||||||
| 9 | Ir | イリジウム | 77 | 7 | 2 | ||||||||||||||||||||
| 10 | Pt | 白金 | 78 | 9 | 1 | 8 | 2 | 1 | |||||||||||||||||
| 11 | Au | 金 | 79 | 10 | 1 | 9 | 2 | 1 | |||||||||||||||||
| 12 | Hg | 水銀 | 80 | 10 | 2 | ||||||||||||||||||||
| 13 | Tl | タリウム | 81 | 10 | 2 | 1 | |||||||||||||||||||
| 14 | Pb | 鉛 | 82 | 10 | 2 | 2 | |||||||||||||||||||
| 15 | Bi | ビスマス | 83 | 10 | 2 | 3 | |||||||||||||||||||
| 16 | Po | ポロニウム | 84 | 10 | 2 | 4 | |||||||||||||||||||
| 17 | At | アスタチン | 85 | 10 | 2 | 5 | |||||||||||||||||||
| 18 | Rn | ラドン | 86 | 10 | 2 | 6 | |||||||||||||||||||
| 第7周期 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | ||||||
| 1 | Fr | フランシウム | 87 | 78 1s … 5d ラドン核 [Rn] | 2 | 6 | 1 | ||||||||||||||||||
| 2 | Ra | ラジウム | 88 | 2 | 6 | 2 | |||||||||||||||||||
| 3 | Ac | アクチニウム | 89 | 2 | 6 | 1 | 2 | 1 | 0 | 2 | |||||||||||||||
| 3 | Th | トリウム | 90 | 2 | 6 | 2 | 2 | 2 | 0 | 2 | |||||||||||||||
| 3 | Pa | プロトアクチニウム | 91 | 2 | 2 | 6 | 1 | 2 | 3 | 0 | 2 | ||||||||||||||
| 3 | U | ウラン | 92 | 3 | 2 | 6 | 1 | 2 | 4 | 0 | 2 | ||||||||||||||
| 3 | Np | ネプツニウム | 93 | 4 | 2 | 6 | 1 | 2 | 5 | 0 | 2 | ||||||||||||||
| 3 | Pu | プルトニウム | 94 | 6 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Am | アメリシウム | 95 | 7 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Cm | キュリウム | 96 | 7 | 2 | 6 | 1 | 2 | 8 | 0 | 2 | ||||||||||||||
| 3 | Bk | バークリウム | 97 | 9 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Cf | カリホルニウム | 98 | 10 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Es | アインスタイニウム | 99 | 11 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Fm | フェルミウム | 100 | 12 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Md | メンデレビウム | 101 | 13 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | No | ノーベリウム | 102 | 14 | 2 | 6 | 2 | ||||||||||||||||||
| 3 | Lr | ローレンシウム | 103 | 14 | 2 | 6 | 2 | 1 | 1 | 0 | 3 | ||||||||||||||
| 4 | Rf (推定) | ラザホージウム | 104 | 14 | 2 | 6 | 2 | 2 | |||||||||||||||||
| 5 | Db (推定) | ドブニウム | 105 | 14 | 2 | 6 | 3 | 2 | |||||||||||||||||
| 6 | Sg (推定) | シーボーギウム | 106 | 14 | 2 | 6 | 4 | 2 | |||||||||||||||||
| 7 | Bh (計算値) | ボーリウム | 107 | 14 | 2 | 6 | 5 | 2 | |||||||||||||||||
| 8 | Hs (推定) | ハッシウム | 108 | 14 | 2 | 6 | 6 | 2 | |||||||||||||||||
| 9 | Mt | マイトネリウム | 109 | 14 | 2 | 6 | 7 | 2 | |||||||||||||||||
| 10 | Ds | ダームスタチウム | 110 | 14 | 2 | 6 | 9 | 1 | 8 | 2 | 1 | ||||||||||||||
| 11 | Rg | レントゲニウム | 111 | 14 | 2 | 6 | 9 | 2 | |||||||||||||||||
| 12 | Cn | コペルニシウム | 112 | 14 | 2 | 6 | 10 | 2 | |||||||||||||||||
| 13 | Nh | ニホニウム | 113 | 14 | 2 | 6 | 10 | 2 | 1 | ||||||||||||||||
| 14 | Fl (推定) | フレロビウム | 114 | 14 | 2 | 6 | 10 | 2 | 2 | ||||||||||||||||
| 15 | Mc (推定) | モスコビウム | 115 | 14 | 2 | 6 | 10 | 2 | 3 | ||||||||||||||||
| 16 | Lv (推定) | リバモリウム | 116 | 14 | 2 | 6 | 10 | 2 | 4 | ||||||||||||||||
| 17 | Ts (計算値) | テネシン | 117 | 14 | 2 | 6 | 10 | 2 | 5 | ||||||||||||||||
| 18 | Og (推定) | オガネソン | 118 | 14 | 2 | 6 | 10 | 2 | 6 | ||||||||||||||||
| 族 | 元素記号 | 元素名 | 原子 番号 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | 6p | 6d | 7s | 7p | |||
| K | L | M | N | O | P | Q | |||||||||||||||||||
| 最大電子数(副殻) | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 14 | 2 | 6 | 10 | 14 | 2 | 6 | 10 | 2 | 6 | ||||||
| 最大電子数(殻) | 2 | 8 | 18 | 32 | 32 | 18 | 8 | ||||||||||||||||||
背景の色=非金属、アルカリ金属、アルカリ土類金属、遷移金属、ハロゲン、貴ガス、典型金属
遷移元素:3~12族、3族のうち原子番号=57~70と原子番号=89~102は内部遷移元素
[貴ガスの元素記号]:電子配置の共通項を簡略形式で表現、例:Se=[Ar],3d10,4s2,4p4
クロム(Cr)と銅(Cu)の電子配置は次の通りです
最外殻電子4sから電子を一つ奪って3d軌道に入っています
●クロム(Cr,24):1s2,2s2,2p6,3s2,3p6,3d5,4s1
d軌道に5個の不対電子が入ることで、スピンが同じ方向を向きエネルギー的に安定化します
(d軌道が半閉殻)
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↑ | ↑ | ↑ | ↑ | |||||||||||||
| 周期4 | N殻 | ↑ | … | ||||||||||||||||||||||||
d軌道に10個の電子対が入ることで、d軌道の電子が全て互いに逆向きスピンで充填され、
エネルギー的に安定化します(d軌道が閉殻)
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||
| 周期4 | N殻 | ↑ | … | ||||||||||||||||||||||||
最外殻電子5sから電子を二つ奪って4d軌道に入っています
●パラジウム(Pd,46):1s2,2s2,2p6,3s2,3p6,3d10,4s2,4p6,4d10,5s0
先に5s軌道から電子が入り始めますが、4d軌道に電子が入り始め4d軌道の電子が増え、
Pdでは5s(↑↓)4d(↑↓)(↑↓)(↑↓)(↑)(↑)ではなく
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||
| 周期4 | N殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↑ | … | |||||||||
| 周期5 | О殻 | ↑ | ↓ | … | |||||||||||||||||||||||
| s軌道 | ┌────p軌道────┐ | ┌──────d軌道──────┐ | ┌───f軌道───┐ | ||||||||||||||||||||||||
| 周期1 | K殻 | ↑ | ↓ | ||||||||||||||||||||||||
| 周期2 | L殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||||||||||||
| 周期3 | M殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ||||||||
| 周期4 | N殻 | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | ↑ | ↓ | … | |||||||
| 周期5 | О殻 | … | |||||||||||||||||||||||||
電子はスピンの向きを揃えたがる性質と、できるだけ離れた電子軌道に入ろうとする二つの重要な性質
があり、最終的に原子全体としていかにバランスよく電子配置するかという観点で電子を配置します
dブロック(3d~6d)の例外1:
d軌道の副殻は、s軌道の副殻から1個の電子(パラジウムの場合は2個)を「借ります」
fブロック(4f~5f)の例外2:
d軌道の副殻は、f軌道の副殻から1個の電子(トリウムの場合は2個)を「借りる」ことがよくあります
pブロック(2p~7p)の例外3:
1970年、ローレンシウム(Lr,103)の基底状態の電子配置は、構造原理に従って、[Rn]5f146d17s2であり、
同族体であるルテチウムの[Xe]4f145d16s2とも合致すると予測された
しかし翌年、この予測に疑義を唱え、その代わり、[Rn]5f147s27p1という異常な電子配置を取るとする
計算結果が公表された
電子の(spdf)軌道とスピン(↑↓)
| 原 子 番 号 | (元素記号)日本語名 | 例外1 例外2 例外3 | 起動順 | 本来は |
|---|---|---|---|---|
| 24 | (Cr)クロム | 1 | 3d5,4s1 | (3d4,4s2) |
| 29 | (Cu)銅 | 1 | 3d10,4s1 | (3d9,4s2) |
| 41 | (Nb)ニオブ | 1 | 4d4,5s1 | (4d3,5s2) |
| 42 | (Mo)モリブデン | 1 | 4d5,5s1 | (4d4,5s2) |
| 44 | (Ru)ルテニウム | 1 | 4d7,5s1 | (4d6,5s2) |
| 45 | (Rh)ロジウム | 1 | 4d8,5s1 | (4d7,5s2) |
| 46 | (Pd)パラジウム | 1 | 4d10,5s0 | (4d8,5s2) |
| 47 | (Ag)銀 | 1 | 4d10,5s1 | (4d9,5s2) |
| 78 | (Pt)白金 | 1 | 5d9,6s1 | (5d8,6s2) |
| 79 | (Au)金 | 1 | 5d10,6s1 | (5d9,6s2) |
| 110 | (Ds)ダームスタチウム | 1 | 6d9,7s1 | (6d8,7s2) |
| 57 | (La)ランタン | 2 | 4f0,5d1 | (4f1,5d0) |
| 58 | (Ce)セリウム | 2 | 4f1,5d1 | (4f2,5d0) |
| 64 | (Gd)ガドリニウム | 2 | 4f7,5d1 | (4f8,5d0) |
| 89 | (Ac)アクチニウム | 2 | 5f0,6d1 | (5f1,6d0) |
| 90 | (Th)トリウム | 2 | 5f0,6d2 | (5f2,6d0) |
| 91 | (Pa)プロトアクチニウム | 2 | 5f2,6d1 | (5f3,6d0) |
| 92 | (U)ウラン | 2 | 5f3,6d1 | (5f4,6d0) |
| 93 | (Np)ネプツニウム | 2 | 5f4,6d1 | (5f5,6d0) |
| 96 | (Cm)キュリウム | 2 | 5f7,6d1 | (5f8,6d0) |
| 103 | (Lr)ローレンシウム | 3 | 6d0,7p1 | (6d1,7p0) |
| 年代 | 物理学者 | アイデア | ||
|---|---|---|---|---|
| 量子論 の誕生 | 1690 | ホイヘンス | 光の波動説 | |
| 17世紀末 | ニュートン | 光の粒子説 | ||
| 19世紀初頭 | ヤング | ヤングの実験 | ||
| 1873 | マクスウェル | 光は電磁波の証明 | ||
| 1888 | ヘルツ | 光電効果を発見 | ||
| 前期量子 論の時代 | 第1期 | 1900年代 | プランク | エネルギー量子仮説 |
| アインシュタイン | 光量子仮説 | |||
| 第2期 | 1910年代 | ラザフォード | 原子核の発見 | |
| ボーア | 原子構造の量子論 | |||
| 現代的な 量子力学 | 第3期 | 1920年代 | ド・ブロイ | 物質波の提唱 |
| ハイゼンベルク | 行列力学 | |||
| シュレディンガー | シュレディンガー方程式 | |||
| ボルン | 物質波は確率の波 | |||
| ハイゼンベルク | 不確定性原理 | |||
| ボーアとハイゼンベルク | コペンハーゲン解釈 | |||
| ディラック | ディラック方程式 | |||
| 量子力学 の発展 | 1930年代~ | エヴェレット | 多世界解釈 | |
| 南部陽一郎 | 対称性の自発的な破れ | |||
| ゲルマンとツヴァイク | クォークモデルを発表 | |||
| ピーター・ヒッグス | ヒッグス機構 | |||
| ワインバーグら | 電弱統一理論 | |||
| ワインバーグと小林・益川 | 標準模型(標準理論) | |||
| ジョージとグラショウ | 大統一理論 | |||
量子論は何人もの天才物理学者がアイデアを出し合って作られた
ホイヘンスの波動説:実体が移動するのでなく、それぞれの地点で振動が起こっている
ニュートンの粒子説:「粒子」という実体がAからBへ移動する
ヤングの二重スリット実験 :光の干渉は波の性質の証拠
マクスウェルの電磁波の予言:光は電磁波の一種である、ヘルツによる電磁波の発見
アインシュタインの光量子説:光電効果は光が粒子なら説明がつく、コンプトン効果
ド・ブロイの物質波 :波と粒子の二面性は光だけでなくほかの物質にもある
コペンハーゲン解釈 :量子は波と粒子の二面性をもつ、量子の相補性
ニュートンの粒子説:「粒子」という実体がAからBへ移動する
ヤングの二重スリット実験 :光の干渉は波の性質の証拠
マクスウェルの電磁波の予言:光は電磁波の一種である、ヘルツによる電磁波の発見
アインシュタインの光量子説:光電効果は光が粒子なら説明がつく、コンプトン効果
ド・ブロイの物質波 :波と粒子の二面性は光だけでなくほかの物質にもある
コペンハーゲン解釈 :量子は波と粒子の二面性をもつ、量子の相補性
「粒子の運動」 ⇒ 「波の塊の移動」
電磁波の「波動性」:波長が長くなるほど、波の回折現象や干渉現象など「波動性」が顕著に表れる
電磁波の「粒子性」:波長が短くなるほど、波の性質が目立たず直進する「粒子性」が顕著に表れる
「粒子性」とは電磁波が数えられることを指し、1個1個のエネルギーの“かたまり”を光子と呼ぶ
光子の運動量p=mc(質量×光速),プランク定数h,波長λ=h/p
光子の質量は0なので質量とエネルギーの等価式E=mc2を用いてm=E/c2,p=E/c,
光子の振動数をνとすると、E=hν,c=νλの関係からp=h/λと変形できます
プランク定数h=6.62607015×10−34Jsは非常に小さいので極微で意味がある
コペンハーゲン解釈:電子の波は電子の発見確率,振幅が大→発見確率が大,振幅が小→発見確率が小
量子の世界の「波と粒子の二重性」は、経験的理解を超え、直観的理解が難しい部分がある
素粒子のスピンの性格、パウリの排他律、トンネル効果、量子もつれ等も同様に難解である
波の性質である波長と粒子の性質であるエネルギーは密接な関係がある
ミクロの世界のエネルギー単位:1eV=1電子を1ボルトで加速時のエネルギー
光子のエネルギーは波長に逆比例する … E=(hc)/λ
3evの紫色の光の波長は0.4ミクロン、2evの赤色の光の波長は0.7ミクロン
電磁波の「粒子性」:波長が短くなるほど、波の性質が目立たず直進する「粒子性」が顕著に表れる
「粒子性」とは電磁波が数えられることを指し、1個1個のエネルギーの“かたまり”を光子と呼ぶ
「粒子性」:位置は精度よく定まるが、波長は不確かになる(波長が短い塊 ⇒ )
「波動性」:波長は精度よく定まるが、位置は不確かになる(波長が長い波 )
光子の実体は、短い(多くの場合数cm~数mの)切れ端のような電磁波(切れ端1個はある波長で振動)「波動性」:波長は精度よく定まるが、位置は不確かになる(波長が長い波 )
光子の運動量p=mc(質量×光速),プランク定数h,波長λ=h/p
光子の質量は0なので質量とエネルギーの等価式E=mc2を用いてm=E/c2,p=E/c,
光子の振動数をνとすると、E=hν,c=νλの関係からp=h/λと変形できます
プランク定数h=6.62607015×10−34Jsは非常に小さいので極微で意味がある
コペンハーゲン解釈:電子の波は電子の発見確率,振幅が大→発見確率が大,振幅が小→発見確率が小
量子の世界の「波と粒子の二重性」は、経験的理解を超え、直観的理解が難しい部分がある
素粒子のスピンの性格、パウリの排他律、トンネル効果、量子もつれ等も同様に難解である
波の性質である波長と粒子の性質であるエネルギーは密接な関係がある
ミクロの世界のエネルギー単位:1eV=1電子を1ボルトで加速時のエネルギー
光子のエネルギーは波長に逆比例する … E=(hc)/λ
3evの紫色の光の波長は0.4ミクロン、2evの赤色の光の波長は0.7ミクロン
特殊相対性理論において、エネルギーEと運動量pの間に、
E=cpなる関係が成立しますので、 … (B)
A式とB式が等価になるためにはA式の質量mは0でなければならないのです
E=mc2という式は物質が消滅(質量=0)すると発生するエネルギーの式で、
アインシュタインがm=E/c2を一般向けに平易に書き換えた式です
E2
――=m2c2+p2なる関係が成立します … (A)
c2
光子の場合、p=mc=E/cからエネルギーEと運動量pの間に――=m2c2+p2なる関係が成立します … (A)
c2
E=cpなる関係が成立しますので、 … (B)
A式とB式が等価になるためにはA式の質量mは0でなければならないのです
E=mc2という式は物質が消滅(質量=0)すると発生するエネルギーの式で、
アインシュタインがm=E/c2を一般向けに平易に書き換えた式です
質量とエネルギーの等価原理
1905年特殊相対性理論
運動を見る視点の側の限定条件:等速運動または静止
光速不変:光の速度はどのような立場から見ても一定である、光よりも速い速度はあり得ない
同時性の破れ:異なる位置における同時性は、慣性系によって変わる(光速不変の原理による)
電車の中央から両壁に光を発射、電車内にいる観測者は両壁到達が同時
外のホームにいる観測者には準光速走行電車の両壁到達は同時ではない
時間の相対性:光の速度に近づくと、時間の流れはゆっくりになる
E=mc2(E:エネルギー、m:質量、c:光速)
質量をエネルギーに、エネルギーを質量に変えられる
1916年一般相対性理論
空間の相対性:重力の大きいところでは空間がゆがむ、大きな重力は光さえも曲げる
時間の相対性:重力の大きいところでは時間の流れはゆっくりになる
運動を見る視点の側の限定条件:等速運動または静止
光速不変:光の速度はどのような立場から見ても一定である、光よりも速い速度はあり得ない
同時性の破れ:異なる位置における同時性は、慣性系によって変わる(光速不変の原理による)
電車の中央から両壁に光を発射、電車内にいる観測者は両壁到達が同時
外のホームにいる観測者には準光速走行電車の両壁到達は同時ではない
時間の相対性:光の速度に近づくと、時間の流れはゆっくりになる
E=mc2(E:エネルギー、m:質量、c:光速)
質量をエネルギーに、エネルギーを質量に変えられる
1916年一般相対性理論
空間の相対性:重力の大きいところでは空間がゆがむ、大きな重力は光さえも曲げる
時間の相対性:重力の大きいところでは時間の流れはゆっくりになる
ファラデーの電磁誘導の法則 磁場が時間変化すると電場が生まれる
アンペールの法則 電流のまわりに磁場ができる
電場のガウスの法則 電場は+電荷から出て-電荷に吸い込まれる(+極/ー極)
磁場のガウスの法則 磁場は湧き出しも吸い込みも起こらない(常にNSペアの場)
アンペールの法則 電流のまわりに磁場ができる
電場のガウスの法則 電場は+電荷から出て-電荷に吸い込まれる(+極/ー極)
磁場のガウスの法則 磁場は湧き出しも吸い込みも起こらない(常にNSペアの場)
2枚の電極→交流電圧→変動する電場→変位電流→変動する磁場発生→変動する電場発生
→2枚の電極のすき間に電場と磁場が交互にあらわれる電磁波が発生し、
周辺に伝わっていく(光:電磁波:電子の往復運動で生じる)
→2枚の電極のすき間に電場と磁場が交互にあらわれる電磁波が発生し、
周辺に伝わっていく(光:電磁波:電子の往復運動で生じる)
電流(電子の流れ)は磁場を作る─┐
├→電磁場の振動=電磁波=光
磁場の変化は電流を作る─────┘
├→電磁場の振動=電磁波=光
磁場の変化は電流を作る─────┘
1900年プランクのエネルギー量子仮説 … (量子論の父)
溶鉱炉の鉄の温度と光の色の研究過程で光のエネルギーはとびとびであることを発見
黒体放射の研究からE=nhν(n=0,1,2,...)という数式を考案(h:プランク定数)
光のエネルギーの量子化、光=波長が連続的な波、を覆す?考え方
νという振動数(色)をもった光はhνの整数倍のエネルギーしか吸収も放射もできない
プランクは光とは言わず「振動子」と呼んでいた
光のエネルギーE,振動数ν,プランク定数h=6.62607015×10−34Js(Js=m2kg/s)
名言 … すべての物質は固有の振動数を持つ
1905年アインシュタインの光量子仮説
プランクのエネルギー量子仮説にヒントを得て光量子仮説を発表
光はエネルギーをもつ粒の集まり、光電効果→光は粒である
1905年は、アインシュタインが3つの大きな発見を発表した奇跡の年です
特殊相対性理論、光量子説に基づく光電効果の理論、ブラウン運動の理論、が
たった一人の物理学者によって提唱されました
100年目の2005年を世界物理年と制定、6月30日はアインシュタイン記念日
光がある一定の波長より短いと金属表面から電子が飛び出し、より長いと電子は飛び出さない
光のエネルギーE,振動数ν,プランク定数h,波長λ,仕事関数Wは金属内の電子取出エネルギー
光量子説:E=hν - W:放出電子のエネルギー最大値、光の粒子の振動数の量子化
・光量子の数を増やす →金属表面から飛び出す電子の数が増える
・光量子の振動数を増やす→金属表面から飛び出す電子のエネルギーが増える
1913年ボーアの原子構造の量子論 … (量子論の育ての親)
1911年、原子の中心には原子核があるとラザフォードが主張した … (原子核物理学の父)
入射したアルファ粒子の偏向からラザフォード散乱による原子核の発見
バルマーは水素ガスに電圧をかけると4色の光の波長に規則性があることに気づいた
ボーアの原子構造の量子論はバルマーの発見の話にヒントを得た
原子核の周りをまわる電子の軌道はとびとびの円軌道
電子の軌道半径Rは必ず次の条件を満たす(p:電子の運動量、n:任意の自然数)
2πRp=nh (n=1:基底状態、h:プランク定数) … ボーアの量子条件
電子が光子を放出・吸収して軌道を飛び移る際に生じる線スペクトルを説明できた
ボーアは量子条件の物理的な意味がわからなかったがその理由を考えたのがド・ブロイ
ラザフォードは後に陽子を発見、中性子の存在を予想、チャドウィックが中性子を発見
1924年ド・ブロイの物質波の提唱
ド・ブロイはボーアの電子のとびとび軌道の直観にボーアに代わってその理由を考えた
アインシュタインの光量子仮説を参考に物質の正体は波であるとして物質波と名付けた
電子の波が消えないためには電子の軌道の1周の長さは波の波長の整数倍に限られる
1周の長さが波長の整数倍、量子条件とは電子の波動性を示すものであった
ド・ブロイが提唱した物質波の概念を知ったシュレディンガーはこれは面白いと思った
1925年ハイゼンベルクの行列力学
量子力学の最初の厳密な定式化
行列力学は量子の世界を粒子の側面から離散的にとらえ、 … ハイゼンベルク
波動力学は量子の世界を波動の側面から連続的にとらえている … シュレディンガー
のちにディラックが発見した変換理論(一般的で抽象的な理論)により行列力学と
波動力学がつなげられ、一方の形式から他方の形式に変換できるようになりました
1925年シュレディンガー方程式の誕生
量子力学の基礎方程式:物質波の方程式
波の高さ(振幅)は複素数の縦軸、面積のような高さをもつ波
波の横軸は電子が存在する場所の広がりを表す
物質波の伝わり方を計算する方程式
波全体がある時刻における1個の電子の状態を表している
角振動数ω=2πν、Ψ=Acos(kx-ωt)+iAsin(kx-ωt)=Aei(kx-wt)
Ψ:座標表示の波動関数(プサイ)は確率振幅を表わす関数(波の高さ)
E:エネルギー固有値
H:ハミルトニアン、位置xと時間t依存運動量の関数=運動エネルギー+位置エネルギー
運動エネルギーT、位置エネルギーV、質量m、全エネルギーE=T+V=H
シュレディンガーの波動方程式は「観測前の波の状態」から、
観測によって「粒子が出現する座標(横軸)の確率(縦軸)」を予測する計算式のことです
1926年ボルンの主張した物質波の正体
シュレディンガーたちは物質波とはどんなものか示せず困っていた
ボルンは物質波の正体は確率の波であるという新たな仮説を主張した
電子のような小さな粒子の観測確率は波動関数の絶対値の2乗に比例する
物質波は確率の波、波動関数を電子位置の確率密度と考える解釈=統計的解釈
ある位置で電子が見出される確率はボルンの規則で与えられる(波動関数の確率解釈)
・波の高いところほど電子が発見される確率が高い
・見られる前の電子はさまざまな場所に広がっている(状態の重ね合わせ)
・見られた途端に波は収縮して電子は1箇所で発見される
P=|Ψ|2、確率P、波動関数Ψ、確率密度関数|Ψ|2 … ボルンの規則
1927年ハイゼンベルクの不確定性原理
ミクロの物質は位置と運動量を同時に確定することができない
電子の位置の測定誤差⊿xは光の波長λの程度
電子の運動量の測定誤差⊿pは⊿x⊿p≧h(プランク定数)/4π
⊿x⊿p≧ħ(ディラック定数)/2
位置と運動量の両者の不確かさを同時になくすのは不可能である
粒子の位置と運動量の測定に、必ず一定以上の不確かさが残ることを示す
運動量演算子pを波動関数ψに作用させ(px-xp)ψを計算すると次式([x,p]:q数)
px-xp=h/(2πi)、x:位置、p:運動量 … ディラックの量子条件
観測者効果ではなく、量子的なゆらぎによるとして改良された小澤の不等式が後日発表された
⊿x⊿p+σx⊿p+σp⊿x≧h/4π … ハイゼンベルクの式に2項追加
σx、σp:物体の位置と運動量が、測定前にもともと持っていた量子ゆらぎ(標準偏差)
1927年コペンハーゲン解釈
ボーアとハイゼンベルクは量子力学における正統的な解釈としても知られる
コペンハーゲン解釈をまとめた(名前の由来はボーア研究所の所在地)
標準解釈:ノイマンが1932年に行った定式化は
・量子系と観測者(観測装置)を分離する(2つの境界はどこに引いても良い)
・量子系の状態は、観測していないときはシュレディンガー方程式に従う
・観測により波動関数が収縮して、1つの測定値が得られる
・どの測定値が得られるかは確率的であり、ボルンの規則に従う
電子の運動はシュレディンガー方程式を満たす波動関数Ψ(r,t)で記述される
波動関数は一般に複素関数で、空間的に広がりを持ち、干渉や回折などの波に特有な性質を現す
電子の位置を実験的に観測した場合には電子はある一点に見出され、広がりを持たない
位置rの周りの微小体積drに電子が発見される確率Pは |Ψ(r,t)|2drに比例する
電子は空間のどこかに存在するはず → ∫Pdr=1 規格化された波動関数
規格化:全空間での積分が1になるような比例定数を見つけるだけの作業、波動関数の調整
電子は波であり粒子である
・波と粒子の両方の性質を取り入れて新しい量子力学の理論が作れる
・電子は観測されないときだけ、波として広がっている
・さまざまな場所にいる状態が重ね合わさってる、状態の重ね合わせ
・電子を観測すると電子の波は一瞬で収縮する
・状態の重ね合わせが解除されて、波が一点に集まり電子は粒子の姿に見える
・波の収縮場所は波動関数の確率解釈で決まる
1928年ディラック方程式
シュレディンガー方程式を特殊相対論の要請を満足するように修正した方程式
ディラックは、この方程式によりコペンハーゲン解釈の問題点を解消させた
溶鉱炉の鉄の温度と光の色の研究過程で光のエネルギーはとびとびであることを発見
黒体放射の研究からE=nhν(n=0,1,2,...)という数式を考案(h:プランク定数)
光のエネルギーの量子化、光=波長が連続的な波、を覆す?考え方
νという振動数(色)をもった光はhνの整数倍のエネルギーしか吸収も放射もできない
プランクは光とは言わず「振動子」と呼んでいた
光のエネルギーE,振動数ν,プランク定数h=6.62607015×10−34Js(Js=m2kg/s)
名言 … すべての物質は固有の振動数を持つ
1905年アインシュタインの光量子仮説
プランクのエネルギー量子仮説にヒントを得て光量子仮説を発表
光はエネルギーをもつ粒の集まり、光電効果→光は粒である
1905年は、アインシュタインが3つの大きな発見を発表した奇跡の年です
特殊相対性理論、光量子説に基づく光電効果の理論、ブラウン運動の理論、が
たった一人の物理学者によって提唱されました
100年目の2005年を世界物理年と制定、6月30日はアインシュタイン記念日
光がある一定の波長より短いと金属表面から電子が飛び出し、より長いと電子は飛び出さない
光のエネルギーE,振動数ν,プランク定数h,波長λ,仕事関数Wは金属内の電子取出エネルギー
光量子説:E=hν - W:放出電子のエネルギー最大値、光の粒子の振動数の量子化
c
c=λν から E=h─ - W 左式によりある一定の波長より短い必要性がわかる
λ
光は量子化された粒子であるとすると光電効果を説明できるc=λν から E=h─ - W 左式によりある一定の波長より短い必要性がわかる
λ
・光量子の数を増やす →金属表面から飛び出す電子の数が増える
・光量子の振動数を増やす→金属表面から飛び出す電子のエネルギーが増える
1913年ボーアの原子構造の量子論 … (量子論の育ての親)
1911年、原子の中心には原子核があるとラザフォードが主張した … (原子核物理学の父)
入射したアルファ粒子の偏向からラザフォード散乱による原子核の発見
バルマーは水素ガスに電圧をかけると4色の光の波長に規則性があることに気づいた
ボーアの原子構造の量子論はバルマーの発見の話にヒントを得た
原子核の周りをまわる電子の軌道はとびとびの円軌道
電子の軌道半径Rは必ず次の条件を満たす(p:電子の運動量、n:任意の自然数)
2πRp=nh (n=1:基底状態、h:プランク定数) … ボーアの量子条件
電子が光子を放出・吸収して軌道を飛び移る際に生じる線スペクトルを説明できた
ボーアは量子条件の物理的な意味がわからなかったがその理由を考えたのがド・ブロイ
ラザフォードは後に陽子を発見、中性子の存在を予想、チャドウィックが中性子を発見
1924年ド・ブロイの物質波の提唱
ド・ブロイはボーアの電子のとびとび軌道の直観にボーアに代わってその理由を考えた
アインシュタインの光量子仮説を参考に物質の正体は波であるとして物質波と名付けた
電子の波が消えないためには電子の軌道の1周の長さは波の波長の整数倍に限られる
1周の長さが波長の整数倍、量子条件とは電子の波動性を示すものであった
ド・ブロイが提唱した物質波の概念を知ったシュレディンガーはこれは面白いと思った
h
2πR=nλ よって pλ=h から λ=── (m:質量、v:速度、p=mv)
mv
2πR=nλ よって pλ=h から λ=── (m:質量、v:速度、p=mv)
mv
1925年ハイゼンベルクの行列力学
量子力学の最初の厳密な定式化
行列力学は量子の世界を粒子の側面から離散的にとらえ、 … ハイゼンベルク
波動力学は量子の世界を波動の側面から連続的にとらえている … シュレディンガー
のちにディラックが発見した変換理論(一般的で抽象的な理論)により行列力学と
波動力学がつなげられ、一方の形式から他方の形式に変換できるようになりました
1925年シュレディンガー方程式の誕生
量子力学の基礎方程式:物質波の方程式
波の高さ(振幅)は複素数の縦軸、面積のような高さをもつ波
波の横軸は電子が存在する場所の広がりを表す
物質波の伝わり方を計算する方程式
波全体がある時刻における1個の電子の状態を表している
角振動数ω=2πν、Ψ=Acos(kx-ωt)+iAsin(kx-ωt)=Aei(kx-wt)
∂Ψ ・
iħ──=iħΨ=HΨ=EΨ … 時間依存型線型偏微分方程式
∂t
i:虚数単位、h:プランク定数、ħ=(h/2π):ディラック定数iħ──=iħΨ=HΨ=EΨ … 時間依存型線型偏微分方程式
∂t
Ψ:座標表示の波動関数(プサイ)は確率振幅を表わす関数(波の高さ)
E:エネルギー固有値
H:ハミルトニアン、位置xと時間t依存運動量の関数=運動エネルギー+位置エネルギー
運動エネルギーT、位置エネルギーV、質量m、全エネルギーE=T+V=H
ħ2 ∂2
H=-──・──+V (x,t)
2m ∂x2
シュレディンガーは彼のアプローチが行列力学と等価であることを示すことができたH=-──・──+V (x,t)
2m ∂x2
シュレディンガーの波動方程式は「観測前の波の状態」から、
観測によって「粒子が出現する座標(横軸)の確率(縦軸)」を予測する計算式のことです
1926年ボルンの主張した物質波の正体
シュレディンガーたちは物質波とはどんなものか示せず困っていた
ボルンは物質波の正体は確率の波であるという新たな仮説を主張した
電子のような小さな粒子の観測確率は波動関数の絶対値の2乗に比例する
物質波は確率の波、波動関数を電子位置の確率密度と考える解釈=統計的解釈
ある位置で電子が見出される確率はボルンの規則で与えられる(波動関数の確率解釈)
・波の高いところほど電子が発見される確率が高い
・見られる前の電子はさまざまな場所に広がっている(状態の重ね合わせ)
・見られた途端に波は収縮して電子は1箇所で発見される
P=|Ψ|2、確率P、波動関数Ψ、確率密度関数|Ψ|2 … ボルンの規則
1927年ハイゼンベルクの不確定性原理
ミクロの物質は位置と運動量を同時に確定することができない
電子の位置の測定誤差⊿xは光の波長λの程度
電子の運動量の測定誤差⊿pは⊿x⊿p≧h(プランク定数)/4π
⊿x⊿p≧ħ(ディラック定数)/2
位置と運動量の両者の不確かさを同時になくすのは不可能である
粒子の位置と運動量の測定に、必ず一定以上の不確かさが残ることを示す
運動量演算子pを波動関数ψに作用させ(px-xp)ψを計算すると次式([x,p]:q数)
px-xp=h/(2πi)、x:位置、p:運動量 … ディラックの量子条件
観測者効果ではなく、量子的なゆらぎによるとして改良された小澤の不等式が後日発表された
⊿x⊿p+σx⊿p+σp⊿x≧h/4π … ハイゼンベルクの式に2項追加
σx、σp:物体の位置と運動量が、測定前にもともと持っていた量子ゆらぎ(標準偏差)
1927年コペンハーゲン解釈
ボーアとハイゼンベルクは量子力学における正統的な解釈としても知られる
コペンハーゲン解釈をまとめた(名前の由来はボーア研究所の所在地)
標準解釈:ノイマンが1932年に行った定式化は
・量子系と観測者(観測装置)を分離する(2つの境界はどこに引いても良い)
・量子系の状態は、観測していないときはシュレディンガー方程式に従う
・観測により波動関数が収縮して、1つの測定値が得られる
・どの測定値が得られるかは確率的であり、ボルンの規則に従う
電子の運動はシュレディンガー方程式を満たす波動関数Ψ(r,t)で記述される
波動関数は一般に複素関数で、空間的に広がりを持ち、干渉や回折などの波に特有な性質を現す
電子の位置を実験的に観測した場合には電子はある一点に見出され、広がりを持たない
位置rの周りの微小体積drに電子が発見される確率Pは |Ψ(r,t)|2drに比例する
電子は空間のどこかに存在するはず → ∫Pdr=1 規格化された波動関数
規格化:全空間での積分が1になるような比例定数を見つけるだけの作業、波動関数の調整
電子は波であり粒子である
・波と粒子の両方の性質を取り入れて新しい量子力学の理論が作れる
・電子は観測されないときだけ、波として広がっている
・さまざまな場所にいる状態が重ね合わさってる、状態の重ね合わせ
・電子を観測すると電子の波は一瞬で収縮する
・状態の重ね合わせが解除されて、波が一点に集まり電子は粒子の姿に見える
・波の収縮場所は波動関数の確率解釈で決まる
1928年ディラック方程式
シュレディンガー方程式を特殊相対論の要請を満足するように修正した方程式
ディラックは、この方程式によりコペンハーゲン解釈の問題点を解消させた
| 量子力学的な現象 | コペンハーゲン解釈 |
|---|---|
| 波と粒子の二重性 | 量子は波の性質と粒子の性質をもつ、同時両有は排除するが相補性がある |
| 不連続性 | 粒子が吸収・放出するエネルギーはとびとび、エネルギーは光子のような量子 |
| 不確定性原理 | 観測が粒子の状態を乱すため、位置と運動のどちらかの正確性が失われる |
| 確率解釈 | 波動関数の絶対値の2乗は粒子の存在確率を示す |
| 重ね合わせ | 観測する迄は波動関数がとり得るさまざまな状態にある |
| トンネル効果 | 反射と透過の重ね合わせ、量子がエネルギーの壁を確率的にすり抜ける現象 |
| 排他原理 | 物質を構成する粒子は、同じ種類が1つの場所に同時には存在しえない |
| 非局所性 | 量子もつれ状態が局所性を破るEPRパラドックス、量子テレポーテーション |
ミクロの世界のルールが判明:ボーア、ボルン、ハイゼンベルグが主張
ルールその1:ミクロの物質のふるまいは、ミクロの物質の正体を波と考えれば説明できる
ルールその2:ミクロの物質のふるまいは、確率的にしかわからない
プランク、アインシュタイン、ド・ブロイ、シュレディンガーは、ルールその2に絶対反対
ルールその1:ミクロの物質のふるまいは、ミクロの物質の正体を波と考えれば説明できる
ルールその2:ミクロの物質のふるまいは、確率的にしかわからない
プランク、アインシュタイン、ド・ブロイ、シュレディンガーは、ルールその2に絶対反対
|
アインシュタインら3名の名前の頭文字からEPRと称し、量子もつれ(絡み合い)状態の非局所 性を指し、量子の状態は特定の状態にはなく、誰かが観測した瞬間にその状態が決まると考える すると、関係しあう2個の量子は、一方の量子の状態が決定すると、はじめて他方の状態も決ま るということが起こり、これらの量子をはるか遠方に引き離してもそれは同じだという |
|
量子エンタングルメント(量子もつれ)は、観測された一方の粒子から、 もう一方に情報が(光速を超えて)伝達されることではなく、 互いに離れた粒子の性質が、セットで決まっていることだと考えられている |
|
送りたい光子状態:光子Xの状態 … 例:水平偏光と垂直偏光の重ね合わせ
↓転送光子準備:EPR対(量子もつれの関係)の光子Aと光子Bの生成 ↓ 光子Bの転送 ↓ 光子Xと光子Aは量子もつれ状態でベル測定(光子Xと光子Aを同時に観測) ↓ 測定結果の古典通信:2ビット値(00,01,10,11)のいずれかを送信(光子Xのズレの補正) ↓ 受信した測定結果から光子Bの偏光操作(補正後の光子B=光子X) ↓ 光子Xの復元(状態情報の復元)
ベル測定:ハーフミラーを用いたビームスプリッターでは、2光子の反射と透過の2種の
組み合わせで4通りあり、この状態を測定することをベル測定と言う 2光子は同時にビームスプリッターに達するようにしなくてはいけない |
量子もつれを生かし、物質の状態をそっくり迅速に遠くへ移すこと
もつれた粒子対(EPR対)の片方を送り手が、他方を受け手がもつ
送り手の粒子を第三の粒子ともつれさせ、この観測結果を通常通信で
受け手に知らせると、その情報を使って受け手の粒子に第三の粒子の
状態を再現できる
もつれた粒子対(EPR対)の片方を送り手が、他方を受け手がもつ
送り手の粒子を第三の粒子ともつれさせ、この観測結果を通常通信で
受け手に知らせると、その情報を使って受け手の粒子に第三の粒子の
状態を再現できる
量子の状態を完全に表現するには波の性質と粒子の性質のどちらも必要
ボーアはこの性質を「相補性」と呼ぶ
位置を特定すると速度が曖昧になり速度を特定すると位置が曖昧になる
という不確定性原理も、相補性の現れであるとされる
ボーアはこの性質を「相補性」と呼ぶ
位置を特定すると速度が曖昧になり速度を特定すると位置が曖昧になる
という不確定性原理も、相補性の現れであるとされる
波の収縮は起こらず、観測された瞬間の波の収縮をシュレディンガー方程式から数学的に導く
ことは原理的に不可能であるとジョン・フォン・ノイマンが証明した
状態の重ね合わせでなく多数の世界の同時存在として説明し直したが多数の世界の同時存在の
証明はできていない(分岐した世界は孤立しているとされている)
ことは原理的に不可能であるとジョン・フォン・ノイマンが証明した
状態の重ね合わせでなく多数の世界の同時存在として説明し直したが多数の世界の同時存在の
証明はできていない(分岐した世界は孤立しているとされている)
ディラックが創始した理論、場の量子化、場の量子論の原型はハイゼンベルクとパウリが創った
従来の量子力学では素粒子が生成・消滅しないものと考え、その座標や運動量を演算子で表すが、
空間の各点での場や粒子数を演算子とし(場の量子化)、その変化を量子論的に追求する理論
これにより素粒子の性質(生成・消滅も含めて)、それらの間の相互作用が統一的に記述される
波または粒子が実在するのではなく、場が振動することで波や粒子に見える
振動が広い範囲で連動すると波に見え、長い時間保持する振動は粒子に見える
力の相互作用はゲージ粒子のキャッチボールではなく、波でもあり粒子でもあるような場の振動
量子電磁力学、量子色力学、電弱相互作用の理論
従来の量子力学では素粒子が生成・消滅しないものと考え、その座標や運動量を演算子で表すが、
空間の各点での場や粒子数を演算子とし(場の量子化)、その変化を量子論的に追求する理論
これにより素粒子の性質(生成・消滅も含めて)、それらの間の相互作用が統一的に記述される
波または粒子が実在するのではなく、場が振動することで波や粒子に見える
振動が広い範囲で連動すると波に見え、長い時間保持する振動は粒子に見える
力の相互作用はゲージ粒子のキャッチボールではなく、波でもあり粒子でもあるような場の振動
量子電磁力学、量子色力学、電弱相互作用の理論
量子論に基づいて宇宙の始まりを考える
ビッグバン宇宙(確実に正しい)
ジョルジュ・ルメートルが宇宙膨張説を発表
エドウィン・ハッブルが膨張宇宙を発見、遠くの銀河ほど遠ざかる、空間自体が膨張
ガモフの火の玉宇宙論(ビッグバン理論)
宇宙マイクロ背景輻射(CMB)の発見:宇宙が昔高温・高密度であった痕跡
WMAP・Planck衛星が描く宇宙創成30万年後の宇宙地図(宇宙の晴れ上がり面)
宇宙マイクロ波背景放射の温度ゆらぎはビッグバン理論の予言と一致
ビッグバン以前(理論的予想)
真空は時空の泡状態で粒子・反粒子が生成・消滅している状態
真空のエネルギーを想定したインフレーション理論など様々なインフレーション理論
ビレンケンの無からの宇宙創成論:量子トンネル効果によって無から極小な宇宙が生まれた
宇宙が虚数の時間に生まれたというホーキングの無境界仮説
誕生直後の宇宙の半径はプランクサイズ→インフレーション→ビッグバン宇宙の誕生
ビッグバン宇宙(確実に正しい)
ジョルジュ・ルメートルが宇宙膨張説を発表
エドウィン・ハッブルが膨張宇宙を発見、遠くの銀河ほど遠ざかる、空間自体が膨張
ガモフの火の玉宇宙論(ビッグバン理論)
宇宙マイクロ背景輻射(CMB)の発見:宇宙が昔高温・高密度であった痕跡
WMAP・Planck衛星が描く宇宙創成30万年後の宇宙地図(宇宙の晴れ上がり面)
宇宙マイクロ波背景放射の温度ゆらぎはビッグバン理論の予言と一致
ビッグバン以前(理論的予想)
真空は時空の泡状態で粒子・反粒子が生成・消滅している状態
真空のエネルギーを想定したインフレーション理論など様々なインフレーション理論
ビレンケンの無からの宇宙創成論:量子トンネル効果によって無から極小な宇宙が生まれた
宇宙が虚数の時間に生まれたというホーキングの無境界仮説
誕生直後の宇宙の半径はプランクサイズ→インフレーション→ビッグバン宇宙の誕生
人間スケール … 古典物理学:力学、電磁気学、熱力学、物性物理・化学、天体物理学・・・
ミクロの世界 … 量子物理学:核物理、素粒子物理、確率解釈、場の量子論、相対論的量子論
宇宙スケール … 相対性理論:4次元時空、重力理論、光速不変、E=mc2
上記3つの物理学領域は一部重なり合っている
ミクロの世界 … 量子物理学:核物理、素粒子物理、確率解釈、場の量子論、相対論的量子論
宇宙スケール … 相対性理論:4次元時空、重力理論、光速不変、E=mc2
上記3つの物理学領域は一部重なり合っている
「量子」は物質ではなく、波動性を持った状態で「エネルギー」として存在していて、
外部からの観測のエネルギーを受けた瞬間に一点に収縮した「粒子」となって出現します
この「エネルギー状態の量子」が外部からの観測のエネルギーを受けた瞬間に一点に収縮
した粒子となって出現する現象のことを波動関数の収縮(=デコヒーレンス)と呼びます
「量子レベルの物質」は実際に観測されたものだけが物質化しており、観測されない限り
「そこにあるかもしれないし、ないのかもしれない」
という『可能性の波』として存在しているということです
「見ていないものは存在すらしないのかもしれない」というような話です
コペンハーゲン解釈は観測できない観測以前の状態を推測して自然界の法則を導こうとする
論理的な仮説でしかなく、そもそもどれが絶対的に正しいという話でもありません
人間は、量子の振る舞いに関するその考え方を正しいか、
間違っているかと判断する手段を持ち合わせていない。
そのような考え方をしたところで実際には何の矛盾も
起きないからこそ採用する。
量子力学は人間の脳が理解できる限界を超えた現象をあるがまま法則として受け入れていると
していますが、とりあえずはそうしておいて、いつの日にか壁を越えて終着駅にたどり着ける
こともかすかに期待しつつ、量子論のおかげで成り立つ最新技術の製品を手にしながら自らを
納得させておきます
外部からの観測のエネルギーを受けた瞬間に一点に収縮した「粒子」となって出現します
この「エネルギー状態の量子」が外部からの観測のエネルギーを受けた瞬間に一点に収縮
した粒子となって出現する現象のことを波動関数の収縮(=デコヒーレンス)と呼びます
「量子レベルの物質」は実際に観測されたものだけが物質化しており、観測されない限り
「そこにあるかもしれないし、ないのかもしれない」
という『可能性の波』として存在しているということです
「見ていないものは存在すらしないのかもしれない」というような話です
コペンハーゲン解釈は観測できない観測以前の状態を推測して自然界の法則を導こうとする
論理的な仮説でしかなく、そもそもどれが絶対的に正しいという話でもありません
人間は、量子の振る舞いに関するその考え方を正しいか、
間違っているかと判断する手段を持ち合わせていない。
そのような考え方をしたところで実際には何の矛盾も
起きないからこそ採用する。
量子力学は人間の脳が理解できる限界を超えた現象をあるがまま法則として受け入れていると
していますが、とりあえずはそうしておいて、いつの日にか壁を越えて終着駅にたどり着ける
こともかすかに期待しつつ、量子論のおかげで成り立つ最新技術の製品を手にしながら自らを
納得させておきます
半導体と量子論 … 半導体の仕組みはバンド理論によって説明できる
光のエネルギーを電気に変換する、電気のエネルギーを光に変換する、
電気の流れを制御できる
情報機器、家電製品、LED電球
超流動と超伝導 … 液体ヘリウムの超流動はボース=アインシュタイン凝縮で説明される
超流動が電子で起こると超伝導と呼ばれ、クーパー対を作った電子は
ボース粒子としてふるまう
超伝導体だけで作った回路は電気抵抗がなくなり永久電磁石になる
リニアモーター
量子コンピュータ … 量子論的な状態の重ね合わせの原理にもとづく量子ビットを用いる
量子もつれ … 量子テレポーテーション
光のエネルギーを電気に変換する、電気のエネルギーを光に変換する、
電気の流れを制御できる
情報機器、家電製品、LED電球
超流動と超伝導 … 液体ヘリウムの超流動はボース=アインシュタイン凝縮で説明される
超流動が電子で起こると超伝導と呼ばれ、クーパー対を作った電子は
ボース粒子としてふるまう
超伝導体だけで作った回路は電気抵抗がなくなり永久電磁石になる
リニアモーター
量子コンピュータ … 量子論的な状態の重ね合わせの原理にもとづく量子ビットを用いる
量子もつれ … 量子テレポーテーション
TOP|未来光円錐|TOP
3次元空間+1次元時間=4次元時空を表現する「光円錐」(の上半分)
事象の地平線(光速の壁)の外側は認識できない領域 = 存在しない?
3次元空間+1次元時間=4次元時空を表現する「光円錐」(の上半分)
光速の傾き 時間 光速の傾き ・←──────────────・──────────────→・ \ ↑ / \ (光速の壁の内側)│(光速の壁の内側) / \ 原点から出発 │ 原点から出発 / \ した光が到達 │ した光が到達 / 事\ し得る範囲 │ し得る範囲 /事 象\ │ /象 の\ │ /の 地\ │時 /地 平\ │間 /平 線\ │の /線 \ │流 / (光速の壁の外側) \ │れ / (光速の壁の外側) 光が届かない \ │ / 光が届かない \ │ / 未来\│/未来 空間・←──────────────●──────────────→・空間 原点
事象の地平線(光速の壁)の外側は認識できない領域 = 存在しない?
| タイトル : 発行所 発行 |
| ・量子論のすべてがわかる本(ptcl) :ワン・パブリッシング 2020年 |
| ・図解相対性理論と量子論(ptcl) : PHP研究所 2006年 |
| ・図解相対性理論と量子論(ptcl) : 学研プラス 2018年 |
|
9.ミクロな粒子 超々微小の物質を構成する素粒子(ptcl) 10.放射線 放射線と原子力、放射性物質、宇宙線(ptcl) 11.元素と周期表 元素記号一覧、周期表、周期表の仕組み、電子配置(ptcl) 12.量子論 ミクロの世界の不思議なルール(ptcl) |
HP作成者:中村三郎,船橋市咲が丘 |